
下列反应符合如图p﹣υ变化曲线的是()

A. H2(g)+I2(g)⇌2HI(g) B. 3NO2(g)+H2O(l)⇌2HNO3(l)+NO(g)
C. 4NH3(g)+5O2(g)⇌4NO(g)+6H2O(g) D. CO2(g)+C(s)⇌2CO(g)
考点: 化学平衡的影响因素.
专题: 化学平衡专题.
分析: 图象分析可知,平衡后增大压强平衡正向进行,正反应速率大于逆反应速率,据此分析判断;
解答: 解:A、H2(g)+I2(g)⇌2HI(g),反应是气体体积不变的反应,增大压强平衡不变,u符合图象变化,故A错误;
B、3NO2(g)+H2O(l)⇌2HNO3(l)+NO(g),反应前后气体体积减小的反应,增大压强平衡正向进行,符合图象变化,故B正确;
C、3NO2(g)+H2O(l)⇌2HNO3(l)+NO(g),反应前后气体体积增大的反应,增大压强,平衡逆向进行,不符合图象变化,故C错误;
D、CO2(g)+C(s)⇌2CO(g),反应前后气体体积增大,增大压强平衡逆向进行,图象不符合变化,故D错误;
故选B.
点评: 本题考查了化学图象分析,平衡移动原理的分析判断,掌握反应特征和平衡移动原理是解题关键,题目较简单.


科目:高中化学 来源: 题型:
一定条件下,化学反应2H2+O2═2H2O的能量变化如图所示,则反应的热化学方程式可表示为()

A. H2(g)+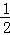 O2(g)═H2O(g)△H=(a+b) kJ•mol﹣1
O2(g)═H2O(g)△H=(a+b) kJ•mol﹣1
B. 2H2(g)+O2(g)═2H2O(g)△H=2(b﹣a) kJ•mol﹣1
C. H2(g)+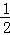 O2(g)═H2O(l)△H=(b+c﹣a) kJ•mol﹣1
O2(g)═H2O(l)△H=(b+c﹣a) kJ•mol﹣1
D. 2H2(g)+O2(g)═2H2O(l)△H=2(a﹣b﹣c) kJ•mol﹣1
查看答案和解析>>
科目:高中化学 来源: 题型:
某实验小组用0.50mol/L NaOH溶液和0.50mol/L硫酸溶液进行中和热的测定.
Ⅰ.配制0.50mol/L NaOH溶液
(1)若实验中大约要使用245mL NaOH溶液,至少需要称量NaOH固体 g.
(2)从图中选择称量NaOH固体所需要的仪器是(填字母): .
名称 托盘天平(带砝码) 小烧杯 坩埚钳 玻璃棒 药匙 量筒
仪器 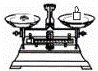

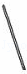

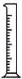
序号 a b c d e f
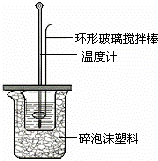
Ⅱ.测定稀硫酸和稀氢氧化钠中和热的实验装置如图所示.
(1)写出该反应的热化学方程式(中和热为57.3kJ/mol): .
(2)取50mL NaOH溶液和30mL硫酸溶液进行实验,实验数据如下表.
①请填写下表中的空白:
温度
实验次数 起始温度t1/℃ 终止温度
t2/℃ 温度差平均值
(t2﹣t1)/℃
H2SO4 NaOH 平均值
1 26.2 26.0 26.1 30.1 4.0
2 27.0 27.4 27.2 33.3
3 25.9 25.9 25.9 29.8
4 26.4 26.2 26.3 30.4
②近似认为0.50mol/L NaOH溶液和0.50mol/L硫酸溶液的密度都是1g/cm3,中和后生成溶液的比热容c=4.18J/(g•℃).则中和热△H= (取小数点后一位).
③上述实验数值结果与57.3kJ/mol有偏差,产生偏差的原因可能是(填字母) .
a.实验装置保温、隔热效果差
b.量取NaOH溶液的体积时仰视读数
c.分多次把NaOH溶液倒入盛有硫酸的小烧杯中
d.用温度计测定NaOH溶液起始温度后直接测定H2SO4溶液的温度.
查看答案和解析>>
科目:高中化学 来源: 题型:
已知某可逆反应:mA(g)+nB(g)⇌pC(g)△H 在密闭容器器中进行,如图所示,反应在不同时间t,温度T和压强P与反应物B在混合气体中的百分含量(B%)的关系曲线,由曲线分析下列判断正确的是()
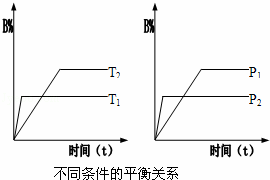
A. T1<T2,p1>p2,m+n<p,△H>0 B. T1>T2,p1<p2,m+n<p,△H<0
C. T1>T2,p1<p2,m+n>p,△H>0 D. T1>T2,p1>p2,m+n>p,△H<0
查看答案和解析>>
科目:高中化学 来源: 题型:
钢铁很容易生锈而被腐蚀,每年因腐蚀而损失的钢铁占世界钢铁年产量的四分之一.请回答钢铁在腐蚀、防护过程中的有关问题.
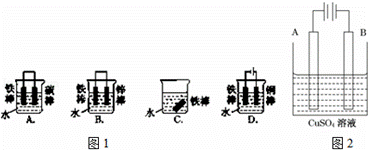
(1)图1哪个装置可防止铁棒被腐蚀BD.
(2)在实际生产中,可在铁 件的表面镀铜防止铁被腐蚀.装置示意图如图2. 请回答
件的表面镀铜防止铁被腐蚀.装置示意图如图2. 请回答
①A电极对应的金属是铜(写元素名称),B电极的电极反应式是 .
②镀层破损后,镀铜铁比镀锌铁更容易被腐蚀,请简要说明原因 .
查看答案和解析>>
科目:高中化学 来源: 题型:
密闭容器中有如下反应:mA(g)+nB(g)⇌pC(g)达到平衡后,保持温度不变,将容器体积缩 小到原来的
小到原来的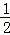 ,当达到新平衡时,C的浓度为原来的1.8倍.下列说法中正确的是()
,当达到新平衡时,C的浓度为原来的1.8倍.下列说法中正确的是()
A. m+n>p B. A的转化率降低
C. 平衡向正反应方向移动 D. C的质量分数增加
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于反应热的说法正确的是()
A. 当△H<0时,表示该反应为吸热反应
B. 已知C(s)+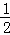 O2(g)=CO(g)△H=﹣110.5kJ/mol,说明碳的燃烧热为110.5kJ/mol
O2(g)=CO(g)△H=﹣110.5kJ/mol,说明碳的燃烧热为110.5kJ/mol
C. 反应热的大小与反应物所具有的能量和生成物所具有的能量无关
D. 化学反应的反应热只与反应体系的始态和终点状态有关,而与反应的途径无关
查看答案和解析>>
科目:高中化学 来源: 题型:
天然水里一般含有Ca2+、Mg2+等多种离子。人们把含有较多量Ca2+、Mg2+的水叫做硬水,含有较少量或不含Ca2+、Mg2+的水叫做软水;降低水中
Ca2+、Mg2+含量的过程叫做硬水软化。如果硬度太高(含Ca2+、Mg2+的浓度太大)会给生产、生活带来很多不利,因此硬水的软化是水处理的重要方面之一。
离子交换法常用于工业锅炉用水的软化。离子交换剂多种多样,磺化煤(NaR)
就是一种阳离子交换剂。
(1)写出用磺化煤软化含Ca2+、Mg2+浓度较高的硬水的离子方程式________
__________________________________________________________________
_________________________________________________________________。
(2)用药剂软化法软化过的水总是含有一定浓度的Ca2+、Mg2+,其原因是
__________________________________________________________________
_________________________________________________________________。
(3)烧水后的锅炉或水壶中结有水垢,据此说明如果用硬度太高的水作锅炉用
水,主要的不利因素是_______________________________________________
_________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列描述正确的是()
A. 氯气、活性炭都能使品红溶液褪色,它们的漂白原理相同
B. 滴加石蕊试液显红色的溶液:Fe3+、NH4+、I﹣可能大量共存
C. 某溶液中加入盐酸酸化的氯化钡产生白色沉淀,原溶液中一定含有SO42﹣
D. Fe(N03)2溶液中滴加少量稀硫酸会变黄色
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com