
【题目】已知,当一个有机物分子中存在两个碳碳双键时,累积双键(如C=C=C)是不稳定的。现有烯烃A(其相对分子质量为84)在一定条件下可以按下面的框图进行反应,B的一卤代物有二种结构。

(F1与F2;G1与G2互为同分异构体)
请填空:
(1)A的结构简式是______________;G1的结构简式是______________
(2)框图中属于取代反应的是________;属于消去反应的是______(填数字代号)。
(3)D在碱性条件下完全水解产物的结构简式是______________________;其(水解产物)含两个碳原子的同系物在浓硫酸、1400C的条件下生成六元环的化学方程式为 ________________________。
【答案】 (CH3)2C=C(CH3)2 BrCH2C(CH3)BrCH(CH3)CH2Br ② ⑤ ![]()
![]()
![]()
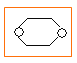 + 2H2O
+ 2H2O
【解析】本题考查有机物的推断,从相对分子质量、反应条件入手,确认官能团, A烯烃,根据单烯烃通式,求出A的分子式为C6H12,A与氢气发生加成反应生成B,即B的分子式为C6H14,B与溴单质,在光照的条件下,发生取代反应,其一溴代物有两种,说明B中有两种不同的氢原子,应是对称结构,则B的结构简式为(CH3)2CH-CH(CH3)2,则A的结构简式为(CH3)2C=C(CH3)2,则D的结构简式为(CH3)2CBr-CBr(CH3)2,然后在氢氧化钠的醇溶液中,发生消去反应,即E的结构简式为CH2=C(CH3)-C(CH3)=CH2,与等物质的量Br2,发生加成反应,其结构简式分别是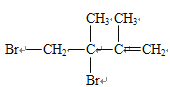 、
、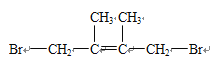 ,前者与HBr发生加成反应,其结构简式为
,前者与HBr发生加成反应,其结构简式为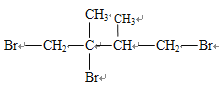 、
、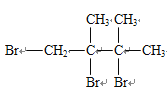 ,后者是
,后者是 ,即G1为:
,即G1为: ,G2为
,G2为 ,(1)根据上述分析,A的结构简式:(CH3)2C=C(CH3)2,G1为:
,(1)根据上述分析,A的结构简式:(CH3)2C=C(CH3)2,G1为: ;(2)属于取代反应的是②;属于消去反应的是⑤;(3)卤代烃在碱的水溶液发生取代反应或水解反应,即水解后的产物是
;(2)属于取代反应的是②;属于消去反应的是⑤;(3)卤代烃在碱的水溶液发生取代反应或水解反应,即水解后的产物是![]() ;两个碳原子,属于同系物,则此有机物为乙二醇,乙二醇在浓硫酸、140℃下发生取代反应,
;两个碳原子,属于同系物,则此有机物为乙二醇,乙二醇在浓硫酸、140℃下发生取代反应,![]()
![]()
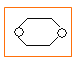 + 2H2O。
+ 2H2O。


科目:高中化学 来源: 题型:
【题目】下列有关阿伏加德罗常数(NA)的说法错误的是( )
A. 22.4L O2所含的原子数目为NA B. 0.5mol H2O含有的原子数目为1.5NA
C. 1mol H2O含有的H2O分子数目为NA D. 05 NA个氯气分子的物质的量是0.5mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验现象,与新制氯水中的某些成分(括号内物质)没有关系的是( )
A.将NaHCO3固体加入新制氯水中,有无色气泡(H+)
B.使红色布条退色(HCl)
C.向FeCl2溶液中滴加氯水,再滴加KSCN溶液,发现呈红色(Cl2)
D.滴加AgNO3溶液生成白色沉淀(Cl﹣)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中正确的是( )
A.NA个N2分子和NA个CO分子的质量之比为1:1
B.水的摩尔质量等于NA个水分子的相对分子质量之和
C.分别由NA个水分子组成的水、冰、水蒸气的质量各不相同
D.1 mol N2的质量等于NA个氮原子的质量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】磷化氢(PH3)、氧硫化碳(COS)均可作储粮害虫杀剂。请回答下列问题:
(1)磷原子的核外电子排布式______,核外有___种不同能量的电子;其最外层有___种运动状态不同的电子,这些电子占据的轨道数为___个。
(2)氧硫化碳中,元素的非金属性最强的元素在周期表中的位置是______;已知COS与CO2的结构相似,试写出COS的电子式_______________,COS属于_____分子(填“极性”或“非极性”)。
(3)用硫酸铜溶液吸收PH3时的化学方程式为:
___CuSO4+ PH3+ H2O→ Cu3P↓+ H3PO4+ H2SO4
(4)配平上述方程式,并标出电子转移方向与数目。
上述反应中氧化剂是______,当吸收2.2molPH3转移电子______mol。
氧硫化碳水解及部分应用流程如下(部分产物已略去):
COS![]() H2S
H2S![]() Na2S
Na2S![]() M溶液+H2
M溶液+H2
(5)写出反应II的离子方程式:_________;
(6)若M溶液中硫元素的存在形式为S2O32﹣,则反应Ⅲ的离子方程式为_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某药物H的合成路线如下图所示,试回答下列问题:
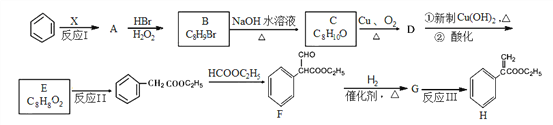
(1)反应Ⅰ中X为烃,其氢的质量分数与苯相同,则X的名称______________。
(2)写结构简式:A__________。D_____________。
(3)写出反应Ⅱ的反应条件:_________________。
(4)写出反应类型:A→B__________。C→D__________。
(5)写出G→H的化学反应方程式:________________________________________。
(6)写出两种满足下列条件的E的同分异构体的结构简式:____________、___________。
①发生银镜反应 ②苯环上有2个取代基 ③属于不同类别的有机物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电镀废水中常含有剧毒的NaCN,可用两段氧化法处理:
①第一段:NaCN+NaClO→NaOCN+NaCl
②第二段:NaOCN+NaClO→Na2CO3+CO2↑+NaCl+N2↑(未配平)
完成下列填空:
(1)上述反应涉及的元素中,氮原子核外未成对电子数是______个;
O2—、Na+、Cl—中半径最小的是_____________。
(2)NaCN晶体中含有的化学键类型为___________________。
(3)第二段过程中,产物属于共价化合物的电子式是___________,其属于__________(填“极性”或“非极性”)分子。
(4)已知:NaOCN中N元素为-3价。配平第二段过程的化学方程式并标出电子转移的方向和数目。_______________
(5)综合两段反应,处理含有0.01 mol NaCN的废水,至少需NaClO________mol。
(6)请用一个方程式证明氮的非金属性大于碳:_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、R、W为五种短周期元素。X原子最外层电子数是核外电子层数的3倍;Y最高正价与最低负价代数和为4;Z的单质常用于漂白工业;R是短周期元素中金属性最强的元素,W是生活中的常见金属,其氧化物常做耐高温材料。回答下列问题:
(1)Y元素的名称______,在周期表中的位于第三周期__________族
(2)W与Z单质化合得到的物质属于__________化合物(选填“离子”或“共价”),向其溶液中加入足量NaOH溶液,反应的离子方程式为______。
(3)工业上常用W单质与氨气在1700℃发生置换反应,生成一种最轻的气体和一种坚硬耐磨的固体,试写出该反应的化学方程式_________________________。
(4)化合物甲由元素X、R组成,甲能与水剧烈反应,并产生大量气泡,写出其化学反应方程式______,甲的电子式为_____________。
(5)为比较元素X和Y的非金属性强弱,下列方法不可行的是___。
a.比较这两种元素的常见单质的沸点
b.比较这两种元素的单质与氢气化合的难易
c.比较这两种元素的气态氢化物的稳定性
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com