
| A、8.1g |
| B、5.4g |
| C、3.6 g |
| D、2.7g |
| 6 |
| 3 |
| 0.3mol |
| x |
| 2 |
| 3 |
| y |
| 0.3mol |


 夺冠金卷全能练考系列答案
夺冠金卷全能练考系列答案科目:高中化学 来源: 题型:
| A、70℃,将0.1 mol 镁粉加入到10 mL 6 mol?L-1 的硝酸溶液中 |
| B、60℃,将0.2 mol 镁粉加入到20 mL 3 mol?L-1 的盐酸溶液中 |
| C、60℃,将0.1 mol 镁粉加入到10 mL 3 mol?L-1 的硫酸溶液中 |
| D、60℃,将0.2 mol 铁粉加入到10 mL 3 mol?L-1 的盐酸溶液中 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Cl2+2Br-═2Cl-+Br2 |
| B、2Fe2++Cl2═2Fe3++2Cl- |
| C、2Fe2++2Br-+2Cl2═2Fe3++4Cl-+Br2 |
| D、2Fe2++4Br-+3Cl2═2Fe3++6Cl-+2Br2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Br2+2I-=I2+2 Br- |
| B、2FeCl2+Cl2=2FeCl3 |
| C、2FeCl2+2HCl+I2=2FeCl3+2HI |
| D、2Fe3++2I-=2Fe2++I2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 常温下 |
| SO2 |
| A、MFe2Ox是还原剂 |
| B、SO2是该反应的催化剂 |
| C、X>Y |
| D、氧化性:MFe2Ox>SO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①②④③ | B、③④①② |
| C、②①④③ | D、④③②① |
查看答案和解析>>
科目:高中化学 来源: 题型:
 ),其过程如下:
),其过程如下: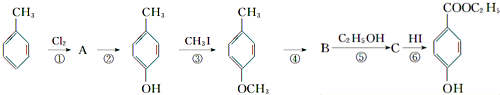
查看答案和解析>>
科目:高中化学 来源: 题型:
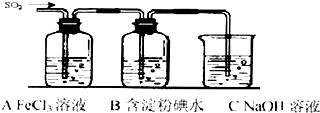
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com