
 »ÆŃ§Ę½ŗā£ŗ
»ÆŃ§Ę½ŗā£ŗ·ÖĪö £Ø1£©·Ö½āĖ®ÖĘĒāĘų£¬ĄūÓĆ·½³ĢŹ½µž¼ÓŹéŠ“×Ü·½³ĢŹ½£¬½įŗĻ“߻ƼĮµÄøÅÄīÅŠ¶ĻĘš“߻ƼĮ×÷ÓƵÄĪļÖŹ£»
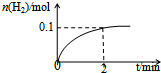
£Ø2£©ÓÉĶ¼æÉÖŖ£¬Ę½ŗāŹ±ĒāĘųµÄĪļÖŹµÄĮæĪŖ0.1mol£¬øł¾Ż·½³ĢŹ½¼ĘĖć²Ī¼Ó·“Ó¦µÄHIµÄĪļÖŹµÄĮ棬ŌŁøł¾Żv=$\frac{\frac{”÷n}{V}}{”÷t}$¼ĘĖćv£ØHI£©£»
£Ø3£©a£®Ń¹ĒæŌö“óĘ½ŗā²»ŅĘ¶Æ£¬HI×Ŗ»ÆĀŹ²»±ä£»
b£®HIµÄĪļÖŹµÄĮæŌö¼Ó£¬HIÅضČŌö“󣬷“Ó¦ĖŁĀŹ¼Óæģ£»
c£®Ōö“óŃ¹Ēæ£¬Ę½ŗā²»ŅĘ¶Æ£¬Ę½ŗāŹ±H2µÄĢå»ż·ÖŹż²»±ä£»
£Ø4£©ZnŗĶĻ”ĮņĖį·“Ó¦Ź±ČÜŅŗÖŠĒāĄė×ÓÅØ¶Č¼õŠ”£¬Ė®µÄµēĄėĘ½ŗāĻņÓŅŅĘ¶Æ£»
a£®¼ÓČėNaNO3£¬²»²śÉśĒāĘų£»
b£®¼ÓČėCuSO4£¬ZnÖĆ»»³öCuŗóŠĪ³ÉŠæĶŌµē³Ų£»
c£®¼ÓČėNa2SO4£¬¶Ō·“Ó¦ĪŽÓ°Ļģ£»
d£®¼ÓČėNaHCO3£¬ŌņČÜŅŗÖŠĒāĄė×ÓÅØ¶Č¼õŠ”£®
½ā“š ½ā£ŗ£Ø1£©·Ö½āĖ®ÖĘĒāĘų£¬ŅŃÖŖ£ŗ
I£ŗSO2+2H2O+I2=H2SO4+2HI£¬
II£ŗ2HI?H2+I2 £¬
¢ó£ŗ2H2SO4=2SO2+O2+2H2O
¹Ź¢ń”Į2+¢ņ”Į2+¢óµĆ£ŗ2H2O=2H2+O2£¬
Õūøö¹ż³ĢÖŠSO2”¢I2²Ī¼Ó·“Ó¦£¬×īŗóÓÖÉś³É£¬ĒŅĮæ²»±ä£¬¹ŹSO2”¢I2ŹĒ“߻ƼĮ£¬
¹Ź“š°øĪŖ£ŗ2H2O=2H2+O2£»ab£»
£Ø2£©ÓÉĶ¼æÉÖŖ£¬Ę½ŗāŹ±ĒāĘųµÄĪļÖŹµÄĮæĪŖ0.1mol£¬ÓÉ·½³ĢŹ½æÉÖŖ²Ī¼Ó·“Ó¦µÄHIµÄĪļÖŹµÄĮæĪŖ0.1mol”Į2=0.2mol£¬¹Źv£ØHI£©=$\frac{\frac{0.2mol}{2L}}{2min}$=0.05mol/£ØL•min£©£¬
¹Ź“š°øĪŖ£ŗ0.05mol/£ØL•min£©£»
£Ø3£©a£®Ń¹ĒæŌö“óĘ½ŗā²»ŅĘ¶Æ£¬HI×Ŗ»ÆĀŹ²»±ä£¬HIµÄĘ½ŗāÅضČĪŖŌĄ“µÄ2±¶£¬¹ŹaÕżČ·£»
b£®HIµÄĪļÖŹµÄĮæŌö¼Ó£¬HIÅضČŌö“󣬷“Ó¦ĖŁĀŹ¼Óæģ£¬“ļµ½Ę½ŗāŹ±¼ä±ČŌĄ“Ėõ¶Ģ£¬¹Źb“ķĪó£»
c£®Ōö“óŃ¹ĒæĘ½ŗā²»ŅĘ¶Æ£¬Ę½ŗāŹ±H2µÄĢå»ż·ÖŹż²»±ä£¬¹Źc“ķĪó£»
¹ŹŃ”a£»
£Ø4£©ZnŗĶĻ”ĮņĖį·“Ó¦Ź±ČÜŅŗÖŠĒāĄė×ÓÅØ¶Č¼õŠ”£¬Ė®µÄµēĄėĘ½ŗāĻņÓŅŅĘ¶Æ£»
a£®¼ÓČėNaNO3£¬²»²śÉśĒāĘų£¬¶ų²śÉśN0£¬¹Źa“ķĪó£»
b£®¼ÓČėCuSO4£¬ZnÖĆ»»³öCuŗóŠĪ³ÉŠæĶŌµē³Ų£¬¼Óæģ·“Ó¦ĖŁĀŹ£¬¹ŹbÕżČ·£»
c£®¼ÓČėNa2SO4£¬¶Ō·“Ó¦ĪŽÓ°Ļģ£¬¹Źc“ķĪó£»
d£®¼ÓČėNaHCO3£¬ŌņČÜŅŗÖŠĒāĄė×ÓÅØ¶Č¼õŠ”£¬·“Ó¦ĖŁĀŹ¼õĀż£¬¹Źd“ķĪó£»
¹Ź“š°øĪŖ£ŗĻņÓŅ£»b£®
µćĘĄ ±¾Ģā×¢Ņāæ¼²é»Æѧ·“Ó¦ĖŁĀŹ¼ĘĖćÓėÓ°ĻģŃĪĖį”¢»ÆŃ§Ę½ŗāµÄÓ°ĻģŅņĖŲµČ£¬ÄѶČÖŠµČ£¬ŹĒ¶Ō»ł“”ÖŖŹ¶µÄ×ŪŗĻĄūÓĆ£¬×¢Ņā¶ŌÖŖŹ¶µÄČ«ĆęÕĘĪÕ£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Ļą¶ŌŌ×ÓÖŹĮæÖš½„Ōö“ó | B£® | ŗĖĶāµē×ÓÅŲ¼³ŹÖÜĘŚŠŌ±ä»Æ | ||
| C£® | ŌŖĖŲµÄ»ÆŗĻ¼Ū³ŹÖÜĘŚŠŌ±ä»Æ | D£® | ŗĖµēŗÉŹżÖš½„Ōö“ó |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ÖÜĘŚ±ķÖŠµÄø÷øöÖ÷×嶼ӊ·Ē½šŹōŌŖĖŲ | |
| B£® | ÖÜĘŚ±ķÖŠµÄø÷øöÖ÷×嶼ӊ½šŹōŌŖĖŲ | |
| C£® | ÖÜĘŚ±ķÖŠµÄ·Ē½šŹōŌŖĖŲ¶¼Ī»ÓŚÖ÷×å£Ø³żĻ”ÓŠĘųĢ壩 | |
| D£® | ÖÜĘŚ±ķÖŠµÄ·Ē½šŹōŌŖĖŲ¶¼Ī»ÓŚ¶ĢÖÜĘŚÄŚ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ¼ī£ŗNaOH”¢KOH”¢Ba£ØOH£©2”¢Na2CO3 | |
| B£® | Ńõ»ÆĪļ£ŗCO2”¢NO”¢SO2”¢H2O | |
| C£® | ļ§ŃĪ£ŗNH4Cl”¢NH4NO3”¢£ØNH4£©2SO4”¢NH3•H2O | |
| D£® | ¼īŠŌŃõ»ÆĪļ£ŗNa2O”¢CaO”¢Mn2O7”¢Al2O3 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
 ½ńÓŠ¼ī½šŹōµÄĮ½ÖÖĢ¼ĖįŃĪŗĶ¼īĶĮ½šŹō£ØµŚ¶žÖ÷×壩µÄŅ»ÖÖ²»ČÜŠŌĢ¼ĖįŃĪ×é³ÉµÄ»ģŗĻĪļ£¬Č”Ęä7.560gÓė¹żĮæŃĪĖįĶźČ«·“Ó¦£¬·Å³öCO2Ģå»żĪŖ1.344L£Ø±źæöĻĀ£©ĮķČ”µČÖŹĮæµÄŌ»ģŗĻĪļ£¬¼ÓĖ®½Į°č£¬æÉĀĖ³ö²»ČÜŠŌŃĪ1.420g£®
½ńÓŠ¼ī½šŹōµÄĮ½ÖÖĢ¼ĖįŃĪŗĶ¼īĶĮ½šŹō£ØµŚ¶žÖ÷×壩µÄŅ»ÖÖ²»ČÜŠŌĢ¼ĖįŃĪ×é³ÉµÄ»ģŗĻĪļ£¬Č”Ęä7.560gÓė¹żĮæŃĪĖįĶźČ«·“Ó¦£¬·Å³öCO2Ģå»żĪŖ1.344L£Ø±źæöĻĀ£©ĮķČ”µČÖŹĮæµÄŌ»ģŗĻĪļ£¬¼ÓĖ®½Į°č£¬æÉĀĖ³ö²»ČÜŠŌŃĪ1.420g£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
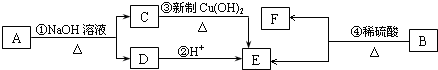
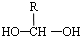 $\stackrel{-H_{2}O}{”ś}$
$\stackrel{-H_{2}O}{”ś}$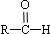 £ØR“ś±ķĢž»ł£©£®
£ØR“ś±ķĢž»ł£©£®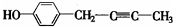 ”¢
”¢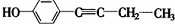 £®
£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
 ijøß¾ŪĪļµÄµ„ĢåA£ØC11H12O2£©æÉ·¢ÉśČēĶ¼±ä»Æ£ŗ
ijøß¾ŪĪļµÄµ„ĢåA£ØC11H12O2£©æÉ·¢ÉśČēĶ¼±ä»Æ£ŗ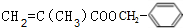 $\stackrel{“߻ƼĮ}{”ś}$
$\stackrel{“߻ƼĮ}{”ś}$ £®
£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
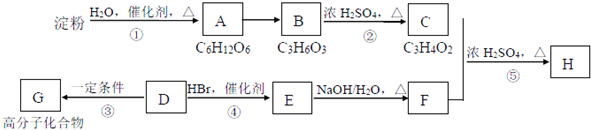
 £»·“Ó¦ĄąŠĶ£ŗ¼Ó¾Ū·“Ó¦£®·“Ó¦¢ÜµÄ»Æѧ·½³ĢŹ½£ŗCH3CH=CH2+HBr$\stackrel{“߻ƼĮ}{”ś}$CH3CHBrCH3£»·“Ó¦ĄąŠĶ£ŗ¼Ó³É·“Ó¦£®
£»·“Ó¦ĄąŠĶ£ŗ¼Ó¾Ū·“Ó¦£®·“Ó¦¢ÜµÄ»Æѧ·½³ĢŹ½£ŗCH3CH=CH2+HBr$\stackrel{“߻ƼĮ}{”ś}$CH3CHBrCH3£»·“Ó¦ĄąŠĶ£ŗ¼Ó³É·“Ó¦£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā

| A£® | 1 mol N2£Øg£©ŗĶ1 mol O2£Øg£©·“Ó¦·Å³öµÄÄÜĮæĪŖ180 kJ | |
| B£® | 1 mol N2£Øg£©ŗĶ1 mol O2£Øg£©¾ßÓŠµÄ×ÜÄÜĮæŠ”ÓŚ2 mol NO£Øg£©¾ßÓŠµÄ×ÜÄÜĮæ | |
| C£® | Ķس£ĒéæöĻĀ£¬N2£Øg£©ŗĶO2£Øg£©»ģŗĻÄÜÖ±½ÓÉś³ÉNO | |
| D£® | NOŹĒŅ»ÖÖĖįŠŌŃõ»ÆĪļ£¬ÄÜÓėNaOHČÜŅŗ·“Ӧɜ³ÉŃĪŗĶĖ® |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com