
【题目】常温下,向20mL 0.2mol/L H2A溶液中滴加0.2 mol/L NaOH溶液,含A元素的有关微粒物质的量变化如下图所示。根据图示判断,下列说法正确的是
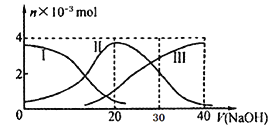
A. H2A在水中的电离方程式是:H2A== H++HA-;HA-![]() H++A2-
H++A2-
B. 等体积等浓度的NaOH溶液与H2A溶液混合后,其溶液中水的电离程度比纯水大
C. 当V(NaOH)=30mL时,溶液中存在以下关系:2c(H+)+ c(HA-)+ 2c(H2A)=c(A2-)+2c(OH-)
D. 当V(NaOH)=20mL时,溶液中各粒子浓度的大小顺序为:c(Na+)>c(HA-)>c(H+)>c(OH-)
【答案】D
【解析】A.0.2molL-1H2A溶液c(H+)<0.4mol/L,则H2A在溶液中部分电离,为弱酸,H2A在水中的电离方程式是:H2AH++HA-、HA-H++A2-,故A错误;B.等体积等浓度的NaOH溶液与H2A溶液混合后生成NaHA,HA-的水解能促进水的电离,故B错误;C.当V(NaOH)=30mL时,发生反应为NaOH+H2A=NaHA+H2O,NaHA+NaOH=Na2A+H2O,溶液主要为等物质量的NaHA,Na2A的混合溶液,根据电荷守恒得:c(Na+)+c(H+)=c(HA-)+2c(A2-)+c(OH-)①,物料守恒可知:3c(HA-)+3c(A2-)+3c(H2A)=2c(Na+)②,①×2+②得:2c(H+)-2c(OH-)=c(A2-)-3c(H2A)-c(HA-),故C正确;D.当V(NaOH)=20 mL时,发生反应为NaOH+H2A=NaHA+H2O,溶液主要为NaHA,HA-电离大于水解,溶液显酸性,则c(Na+)>c(HA-)>c(H+)>c(A2-)>c(OH-),故D正确;故选D。


 口算心算速算应用题系列答案
口算心算速算应用题系列答案 同步拓展阅读系列答案
同步拓展阅读系列答案科目:高中化学 来源: 题型:
【题目】用括号内试剂及操作方法除去下列各物质中的少量杂质,不正确的是( )
A. 二氧化碳中的氯化氢(饱和碳酸钠溶液、洗气)
B. 乙酸乙酯中的乙酸(饱和碳酸钠溶液、分液)
C. 溴乙烷中的乙醇(水、分液)
D. 溴苯中的溴(NaOH溶液、分液)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、W为元素周期表前四周期的元素。其中X是形成化合物种类最多的元素,Y的内层电子数是最外层电子数的9倍,Z是元素周期表中电负性最大的元素,W元素的第三电子层处于全充满状态且第四电子层只有2个电子。请回答下列问题。
(1)W元素在元素周期表中的位置为______________________________。
(2)W2+能与氨气分子形成配离子[W(NH3)4]2+。写出该配离子的结构简式(标明配位键)_______。
(3)X能与氢、氮、氧三种元素构成化合物XO(NH2)2,其中X原子的杂化方式为__________,1mol该分子中σ键的数目为______________,该物质易溶于水的主要原因是________________。
(4)X的某种晶体为层状结构,可与熔融金属钾作用。钾原子填充在各层之间,形成间隙化合物,其常见结构的平面投影如图①所示,则其化学式可表示为______________________。
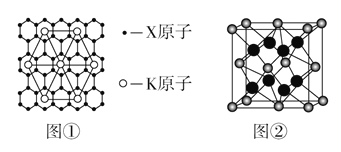
(5)元素Y与元素Z形成的晶胞结构如图②所示,该晶胞中Y离子周围最近的Z的离子为___个。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上以钛铁矿[主要成分为钛酸亚铁(FeTiO3),含有MgO、SiO2等杂质]为原料,制备金属钛和铁红的工艺流程如下:

已知:①酸酸时,FeTiO3转化为Fe2+和TiO2+ ;
②本实验温度下,Ksp[Mg(OH)2]=1.0×10-11;
③溶液中离子浓度小于等于l .0×10-5mol/L时,认为该离子沉淀完全。
请国答下列问题:
(1)FeTiO3中Ti元素的化合价为_____价,铁红的用途为_____(任写一种)。
(2)“水解”中,发生反应的离子方程式为________。
(3)“沉铁”中,气态产物的电子式为______;该过程需控制反应温度低于35 ℃,原因为_______。
(4)FeCO3转化为铁红时,发生反应的化学方程式为____________。
(5)滤液3可用于制备Mg(OH)2。若滤液3中c(Mg2+)=1.2×10-3mol/L,向其中加入等体积的NaOH溶液的浓度为________ mol/L时,可使Mg2+恰好沉淀完全(溶液体积变化忽略不计)。
(6)“电解”时,电解质为熔融的CaO,则阴极反应式为_______,制得1molTi单质,理论上导线中通过的电量为______(保留三位有效数字,已知:l 个电子的电量为1.6×10-19C ) 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】正硼酸(H3BO3)是一种片层状结构白色晶体,层内的H3BO3分子通过氢键相连(如下图)。下列有关说法正确的有

A. 在H3BO3分子中各原子最外层全部满足8电子稳定结构
B. H3BO3分子的稳定性与氢键有关
C. 1mol H3BO3的晶体中有3mol极性共价键
D. 1mol H3BO3的晶体中有3mol氢键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列事实不能用勒夏特列原理解释的是( )
A. 溴水中有下列平衡Br2+H2O![]() HBr+HBrO,当加入硝酸银溶液后,溶液颜色变浅
HBr+HBrO,当加入硝酸银溶液后,溶液颜色变浅
B. 已知, N2 (g) + 3 H2(g)![]() 2NH3(g) △H﹤0 ,为提高氨的产率,理论上应采取降低温度的措施
2NH3(g) △H﹤0 ,为提高氨的产率,理论上应采取降低温度的措施
C. 反应CO(g)+NO2(g)![]() CO2(g)+NO(g)△H﹤0,达平衡后,升高温度体系颜色变深
CO2(g)+NO(g)△H﹤0,达平衡后,升高温度体系颜色变深
D. 对于2HI(g)![]() H2(g)+I2(g),达平衡后,缩小容器体积可使体系颜色变深
H2(g)+I2(g),达平衡后,缩小容器体积可使体系颜色变深
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列对X+2Y=X2++2Y-的叙述中正确的是
A.Y被还原,X2+是还原产物 B.Y被还原,X发生氧化反应
C.X是还原剂,Y被氧化 D.X被氧化,X显氧化性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一学习小组利用下图所示装置,对某含少量Fe的废铜屑进行铜含量的测定,并探究利用其制备硫酸铜溶液。

(1)向A中加入10g废铜屑样品,关闭弹簧夹,打开B活塞向A注入足量稀硫酸后关闭。①此时装置C中产生的现象是 。
②反应进行到A中不再产生气泡时,若C中收集到448mL(已换算成标准状况)气体,则该废铜屑中铜的质量百分含量为 。
(2)接下来使Cu完全溶解的操作是:
① 拆除C、D装置后,打开弹簧夹
②____________________________________________________________________
(3)为使A中固体加快溶解速率,以下方法运用合理的是 。
a.对A装置加热;b.向A内加入少量Fe2O3;c.向A内加入少量CuO;d.增大空气通入量;e.向A内加入少量FeSO4;f.向A内加入少量H2O
(4)将A中溶液倒入烧杯内,加入Cu2(OH)2CO3将其调节至pH=4时,溶液中铁元素被完全沉淀,过滤后即得红褐色沉淀与硫酸铜溶液。
①此过程的离子反应方程式是 。
②检验溶液中铁元素是否被完全沉淀最好的方法是___________
a.取样于试管→滴加KSCN溶液
b.取样于试管→滴加酸性KMnO4溶液
c.取样于试管→纸上层析后→ 喷KSCN溶液;
(5)有同学认为,可以不用测量气体法计算废铜屑中铜的质量百分含量,其具体操作步骤可续写为: 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com