
【题目】NA代表阿伏加德罗常数的值。下列说法正确的是( )
A.124g的P4含有P-P键的数目为6NA
B.15.6g的苯含有σ键的数目为1.2NA
C.2.24L的乙炔含有π键的数目为0.2NA
D.60g的SiO2中含有Si-O键的数目为2NA
 文敬图书课时先锋系列答案
文敬图书课时先锋系列答案科目:高中化学 来源: 题型:
【题目】X、Y、Z、W是原子序数依次增大的前四周期元素,X、Z的周期序数=族序数,由这四种元素组成的单质或化合物存在如图所示的转化关系,其中甲、戊是两常见的金属单质,丁是非金属单质,其余为氧化物且丙为具有磁性的黑色晶体。下列说法正确的是

A. W的原子序数是Z的两倍,金属性强于Z
B. W元素在周期表中的位置是第四周期VIII族
C. 丙属于两性氧化物
D. 等物质的量的甲和戊完全溶于稀硝酸,消耗的HNO3的量一定相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】节日期间因燃放鞭炮会引起空气中SO2含量增高,造成大气污染。某实验小组同学欲探究SO2的性质,并测定空气中SO2的含量。
(1)他们设计如下实验装置,请你参与探究,并回答问题:
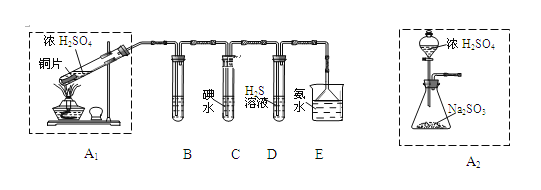
①装置A1中发生反应的化学方程式为_______;
②装置B用于检验SO2的漂白性,其中所盛试剂为_____,装置D用于检验SO2的_______性质;
③装置C中反应的离子方程式为_____;
④为了实现绿色环保的目标,甲同学欲用装置A2代替装置A1,你认为装置A2的优点是(写一点即可)_____________________;
(2)他们拟用以下方法测定空气中SO2含量(假设空气中无其他还原性气体、实验在标准状况下测定)。
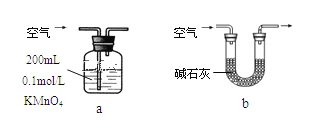
你认为哪个装置可行(填序号)______,使用你所选用的装置测定SO2含量时,还需要测定的物理量是_____________________________;
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氨基甲酸铵(NH2COONH4)是治疗某种疾病的重要成分,也可用作肥料。氨基甲酸铵是一种白色固体,易分解、易水解,难溶于CCl4。实验小组设计在实验室中用氨气和二氧化碳反应制备氨基甲酸铵。
(1)氨气的制备
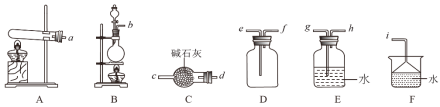
①实验室制取氨气的发生装置可以选择图中的__,反应的化学方程式为__。
②欲收集一瓶干燥的氨气,选择图中的装置,其连接顺序为:发生装置→__。(按气流方向,用小写字母表示)。
(2)氨基甲酸铵(NH2COONH4)的制备把氨气和二氧化碳通入四氯化碳中,不断搅拌混合,生成的氨基甲酸铵小晶体悬浮在四氯化碳中。当悬浮物较多时,停止制备。制备氨基甲酸铵的装置和反应的化学方程式如下:2NH3(g)+CO2(g)![]() NH2COONH4(s) △H<0。
NH2COONH4(s) △H<0。
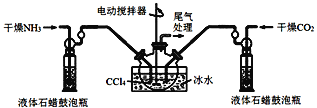
注:四氯化碳与液体石蜡均为惰性介质。
①发生器用冰水冷却的目的是___。
②液体石蜡鼓泡瓶的作用是__。
③从反应后的混合物中分离出产品的方法是__(填写操作名称)。
④尾气处理装置如图所示,装置中的浓硫酸的作用除了用于阻止空气中水蒸气进入反应器使氨基甲酸铵水解,还用于__。
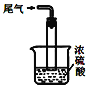
⑤取因部分变质而混有碳酸氢铵的氨基甲酸铵样品0.7820g,用足量石灰水充分处理后,使碳元素完全转化为碳酸钙,过滤、洗涤、干燥,测得质量为1.000 g。则样品中氨基甲酸铵的物质的量分数为__。(精确到2位小数,碳酸氢铵和氨基甲酸铵的相对分子质量分别为79和78)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】0.10 mol镁条在只含有CO2和O2混合气体的容器中燃烧(产物不含碳酸镁),反应后容器内固体物质的质量不可能为( )
A. 3.2 g B. 4.0 g C. 4.2 g D. 4.6 g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于有机物的结构和性质的叙述正确的是( )
A.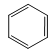 、
、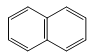 、
、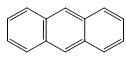 互为同系物
互为同系物
B.乙烯和聚乙烯均可使酸性高锰酸钾溶液褪色
C.苯分子的一个H原子被—C4H9取代后的产物共有4种
D.丙烷是直链烃,所以分子中3个碳原子在一条直线上
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列内容与结论相对应的是
选项 | 内容 | 结论 |
A | H2O(g)变成H2O(l) | △S>0 |
B | 硝酸铵溶于水可自发进行 | 因为△S>0 |
C | 一个反应的△H>0,△S>0 | 反应一定不自发进行 |
D | H2(g)+F2(g)=2HF(g),△H=-271kJ/mol △S=8J/(mol·K) | 反应在任意外界条件下均可自发进行 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为探究矿石样品A(仅含两种元素)的组成和性质,设计并完成如下实验:

已知溶液D中只含一种金属阳离子,与铁粉充分反应后固体质量减少14 g。
请回答:
(1)样品A的化学式为________________。
(2)写出气体c与溴水反应的离子方程式___________________。
(3)写出样品A与盐酸发生氧化还原反应的化学方程式____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用双线桥标出下列反应电子转移的方向和数目,并指出氧化剂、还原剂和氧化产物、还原产物。
①2KMnO4 + 16HCl=2KCl + 2MnCl2+ 5Cl2↑ + 8H2O_________。
氧化剂(___________)、还原剂(___________)、氧化产物(____________)、还原产物(____________)。
②H2S + H2SO4=S↓+ SO2↑+ 2H2O_______________。
氧化剂(___________)、还原剂(___________)、氧化产物(____________)、还原产物(____________)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com