
����Ŀ��ijͬѧ������ͼװ�ý���ʵ�飬֤����ͭ��ϡ���ᷴӦ������NO��ʵ��ʱ������ע�����ڼ���һ������ϡ���ᣬ�ž�ע�����ڵĿ�����Ѹ�ٽ�����ͭ˿����Ƥñ���ϣ�һ��ʱ���ע����������ɫ���������

��1��ͭ��ϡ���ᷴӦ�Ļ�ѧ����ʽΪ_________________��
��2��NO�Ǵ�����Ⱦ��֮һ��Ŀǰ��һ��������������400�����ҡ��д������ڵ�����£��ð�����NO��ԭΪ������ˮ���÷�Ӧ�Ļ�ѧ����ʽΪ4NH3+6NO![]() 5N2+6H2O��ÿ��5 mol N2���ɣ����������뻹ԭ��������ʵ���֮��Ϊ__________��
5N2+6H2O��ÿ��5 mol N2���ɣ����������뻹ԭ��������ʵ���֮��Ϊ__________��
��3����������ϡ���ỻ��Ũ���ᣬ�����ɵ�����ͨ��ˮ�У���������ˮ��Ӧ�Ļ�ѧ����ʽΪ______________________________________________��
��4����д��ʵ������NH4Cl��Ca(OH)2������ȡ�����Ļ�ѧ����ʽ__________��
��������Ȫʵ�飬����ˮ�м����̪���õ���ɫ��Ȫ����ʵ�������˰�����������Ҫ���ʷֱ���________________________��___________________________��
���𰸡�3Cu+8HNO3(ϡ)===3Cu(NO3)2+2NO��+4H2O 2��3 3NO2+H2O===2HNO3+NO 2NH4Cl+Ca(OH)2![]() CaCl2+2NH3��+2H2O ����������ˮ ������ˮ��Ӧ���ɼ�
CaCl2+2NH3��+2H2O ����������ˮ ������ˮ��Ӧ���ɼ�
��������
(1)ͭ��ϡ���ᷴӦ����NO����,��Ӧ�Ļ�ѧ����ʽΪ3Cu+8HNO3(ϡ)===3Cu(NO3)2+2NO��+4H2O ,��ˣ�������ȷ����: 3Cu+8HNO3(ϡ)===3Cu(NO3)2+2NO��+4H2O ;
(2)��Ӧ4NH3+6NO![]() 5N2+6H2O����,NOΪ������,N2Ϊ��ԭ��� NH3Ϊ��ԭ��, N2Ϊ����������ݷ���ʽ��֪��ÿ����5molN2,��6molNO����ԭ, 4molNH3�����������������뻹ԭ��������ʵ���֮��Ϊ2:3����ȷ������2��3��
5N2+6H2O����,NOΪ������,N2Ϊ��ԭ��� NH3Ϊ��ԭ��, N2Ϊ����������ݷ���ʽ��֪��ÿ����5molN2,��6molNO����ԭ, 4molNH3�����������������뻹ԭ��������ʵ���֮��Ϊ2:3����ȷ������2��3��
(3)ͭ��Ũ���ᷴӦ����NO2, NO2����ˮ��Ӧ���������NO,��Ӧ�ķ���ʽΪ3NO2+H2O===2HNO3+NO,��ˣ��������: 3NO2+H2O===2HNO3+NO��
��4����ʵ������NH4Cl��Ca(OH)2������ȡ�����Ļ�ѧ����ʽ2NH4Cl+Ca(OH)2![]() CaCl2+2NH3��+2H2O����: 2NH4Cl+Ca(OH)2
CaCl2+2NH3��+2H2O����: 2NH4Cl+Ca(OH)2![]() CaCl2+2NH3��+2H2O��
CaCl2+2NH3��+2H2O��
���ܽ�����Ȫʵ�飬˵������������ˮ������ˮ�м����̪���õ���ɫ��Ȫ��˵������ˮ��Һ�Լ��������Ը�ʵ�������˰���������ˮ��������ˮ��Ӧ���ɼ�𰸣�����������ˮ�� ������ˮ��Ӧ���ɼ���



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ HCl��HBr��HI��������Է����������������ǿ���� ( )
A. ���ۼ��ļ���B. �⻯����ȶ���C. ���»���D. ���ۼ��ļ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��̼�ǵ���������������������Ԫ��֮һ������Ҫ��ش���������:
��1��̼ԭ�ӵļ۵����Ų�ͼ��________________��������______�ֲ�ͬ�˶�״̬�ĵ��ӡ�
��2��̼�����γɶ����л��������ͼ��ʾ��һ�����ʺ�һ����वĽṹ�����ַ���������ԭ�Ӷ���һ��ƽ���ϡ�

������������Ԫ�صĵ縺���ɴ�С��˳��______________________��
�������й��֮��ļнǡ�1�ȡ�2����ԭ��_________________________________��
����ऽṹ��N ԭ�ӵ��ӻ���ʽ___________��
�ܷ����еĴ�м������÷���![]() ��ʾ������m���������γɴ�м���ԭ������n���������γɴ�м��ĵ�����(�籽�����еĴ�м��ɱ�ʾΪ
��ʾ������m���������γɴ�м���ԭ������n���������γɴ�м��ĵ�����(�籽�����еĴ�м��ɱ�ʾΪ![]() )�������ʺ�����ж����д�м������ʸ�����еĴ�м���ʾΪ______________��
)�������ʺ�����ж����д�м������ʸ�����еĴ�м���ʾΪ______________��
��3��̼���γ�CO��CO2��H2CO3�ȶ����������
���ڷ�ӦCO ת����CO2 �Ĺ����У�����˵����ȷ����__________��
A��ÿ�������й¶Ե��������� B�����Ӽ��Ա仯
C��ԭ�Ӽ�ɼ���ʽ�ı� D�����ӵ��۷е���
�ڸɱ��ͱ������ֳ����ķ��Ӿ��壬�����еĿռ������ʣ��ɱ�_______����(�>���� ��<����=��)
��H2CO3��H3PO4����1�����ǻ�����H3PO4Ϊ��ǿ�ᣬH2CO3Ϊ�����ԭ��___________��
��4����2017 �꣬�����ѧ���Ŷӹ�ͬ�ϳ���̼��һ������ͬ�������壺 T- ̼��T- ̼�Ľṹ�ǣ����������ʯ�е�ÿ��̼ԭ����һ����4 ��̼ԭ����ɵ���������ṹ��Ԫȡ�����γ�̼��һ��������ά��������ṹ������ͼ����֪T- ̼��������Ϊa pm������٤������ΪNA����T- ̼���ܶȵı���ʽΪ______________g/cm3��

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������£�0.1 mol/L��H2C2O4��Һ��H2C2O4��HC2O4-��C2O42-��������ռ���ʵ����������ֲ�ϵ������pH�仯�Ĺ�ϵ����ͼ��ʾ�����б�������ȷ����
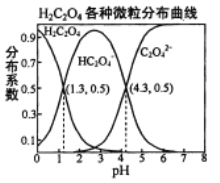
A. HC2O4-![]() H+��C2O42-��K��1��10-4.3
H+��C2O42-��K��1��10-4.3
B. �������ʵ�����NaHC2O4��Na2C2O4����ˮ����������ҺpHǡ��Ϊ4.3
C. ������HF��K��1��10-3.4��������H2C2O4��Һ���뵽����NaF��Һ���������ķ�ӦΪ��H2C2O4��F-��HF��HC2O4-
D. ��0.1 mol/L NaHC2O4��Һ����������Ũ�ȴ�С��ϵΪ��c(Na+)��c(HC2O4-)��c(H+)��c(C2O42-)��c(OH-)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����б仯�У�����������������ܷ�������
A. SO2��S B. Cl2��HClO C. Fe2+��Fe3+ D. HCO3-��CO32-
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��A��B��C��D������ѧ��ѧ�г��������ʣ�����A��B��C������ͬһ��Ԫ�أ���һ���������ת����ϵ���£����ַ�Ӧ�е�ˮ����ȥ������������ش��������⣺

��1����A��B��C����ɫ��Ӧ��Ϊ��ɫ��CΪ���ͷ۵ijɷ�֮һ��D�Ĺ����ŷŻ��������ЧӦ��
��B������Ϊ_______________��
����Ӧ�������ӷ���ʽ��_________________________________________��
��2����A��D��Ϊ���ʣ���AΪ���壬DԪ�ص�һ�ֺ���ɫ�����ﳣ�������ϡ�
��д��A��һ����;_________________________��
�ڷ�Ӧ�������ӷ���ʽ��_________________________________________��
�ۼ���B����Һ�������ӵķ�����________________________________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������ѣ�Ti������Ϊ21���ͽ������䵥�ʺͻ�������й㷺��Ӧ�ü�ֵ����ش��������⣺
��1��Ti�Ļ�̬ԭ�Ӽ۵����Ų�ʽΪ______��
��2������TiO2������������Ӧ�Ĵ�����

������ķ����в�ȡsp2��ʽ�ӻ���̼ԭ����_____�������������в�ȡsp3��ʽ�ӻ���ԭ�Ӷ�ӦԪ�صĵ縺���ɴ�С��˳��Ϊ_____��
��3��ij��Ti3+�����Ļ�ѧʽΪ[TiCl(H2O)5]Cl2��H2O��������������к��еĻ�ѧ��������_____��1 mol��������к��е�������Ŀ��_____��
��4��ͨ��x������֪̽KCl��MgO��CaO��TiN�ľ�����NaCl�ľ���ṹ���ƣ���֪�������Ӿ���ľ������������£�
���Ӿ��� | NaCl | KCl | CaO |
������/kJ��mol��1 | 786 | 715 | 3401 |
KCl��MgO��CaO��TiN�������Ӿ����۵��ɸߵ��͵�˳��Ϊ_____��
��5��������������ͬ�������壬�������������ѻ��������������������ѻ�����ͼ��ʾ���Ѿ����һ�־�������������a��0.469 nm��c��0.295 nm������Ѿ�����ܶ�Ϊ______g��cm-3����NA ��ʾ�����ӵ�������ֵ���г�����ʽ���ɣ���

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������������ڴ��ᡢ�����ƻ����Һ�У���c(CH3COOH)+c(CH3COO-)=0.lmol.L-1ʱ��c(CH3COOH)��c(CH3COO-)��pH�Ĺ�ϵ��ͼ��ʾ�������й�������ȷ����

A��pH=5.5����Һ�У�c(CH3COOH)>c(CH3COO��)>c(H+)>c(OH-)
B����W������ʾ��1.0L��Һ��ͨ��0.05molHCl���壨��Һ����仯�ɺ��ԣ���c(H+)=c(CH3COOH)+c(OH-)
C��W������ʾ����Һ�У�c(Na+)+c(H+)=c(CH3COOH)+c(OH)-
D��pH=3.5����Һ�У�c(Na+)+c(H+)+c(OH-)+c(CH3COOH)=0.1mol��L-l
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һ�������£����ڿ��淴Ӧ��X(g)��3Y(g) ![]() 2Z(g)����X��Y��Z����ʼŨ�ȷֱ�Ϊc1��c2��c3������Ϊ�㣩���ﵽƽ��ʱ��X��Y��Z��Ũ�ȷֱ�Ϊ0.1 mol��L��1��0.3 mol��L��1��0.08 mol ��L��1���������ж���ȷ���ǣ� ��
2Z(g)����X��Y��Z����ʼŨ�ȷֱ�Ϊc1��c2��c3������Ϊ�㣩���ﵽƽ��ʱ��X��Y��Z��Ũ�ȷֱ�Ϊ0.1 mol��L��1��0.3 mol��L��1��0.08 mol ��L��1���������ж���ȷ���ǣ� ��
A. c1��c2��1��3
B. ƽ��ʱY��Z����������֮��Ϊ2��3
C. X��Y��ת����֮��Ϊ1��3
D. c1��ȡֵ��ΧΪ0.04 mol��L��1��c1��0.14 mol��L��1
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com