
下列各组离子在溶液中能够大量共存,当溶液中c(H+)=10-1 mol·L-1时有气体产生;而当溶液中c(H+)=10-13 mol·L-1时又能生成沉淀。则该组离子可能是
A.Na+、Ba2+、NO3―、CO32―
B.Fe2+、Na+、SO42―、NO3―
C.Mg2+、NH4+、SO42-、Cl-
D.Ba2+、K+、Cl-、NO3―
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:2015-2016学年重庆市高一上学期第一次月考化学试卷(解析版) 题型:填空题
(4分)下列所含分子数由多到少的排列顺序是 。
A.标准状况下33.6 L H2
B.所含电子的物质的量为4 mol的H2
C.20 ℃时45 g H2O
D.常温下,16 g O2与14 g N2的混合气体
E.含原子总数约为1.204×1024的NH3
查看答案和解析>>
科目:高中化学 来源:2016届浙江省高三上学期10月阶段测化学试卷(解析版) 题型:选择题
将51.2gCu完全溶于适量浓硝酸中,收集到氮的氧化物(含NO、N2O4、NO2)的混合物共0.8mol,这些气体恰好能被500ml 2mol/LNaOH溶液完全吸收,生成含NaNO3和NaNO2的盐溶液,其中NaNO2的物质的量为
(已知NO+NO2+2NaOH===2NaNO2+H2O,2NO2+2NaOH===NaNO3+NaNO2+H2O)
A.0.8mol B.0.6mol C.0.2mol D.1.0mol
查看答案和解析>>
科目:高中化学 来源:2016届浙江省高三上学期第一次月考化学试卷(解析版) 题型:选择题
判断下列有关化学基本概念的依据正确的是
A.溶液与胶体:本质不同的原因是能否发生丁达尔效应
B.共价化合物:是否含有共价键
C.强弱电解质:溶液的导电能力大小
D.氧化还原反应:元素是否发生电子转移
查看答案和解析>>
科目:高中化学 来源:2016届湖南省益阳市高三上学期第三次模拟化学试卷(解析版) 题型:选择题
右表是元素周期表的一部分,X、Y、Z、W均为短周期元素,下列说法不正确的是
X | Y | ||
Z | W |
A.原子半径:Z>X>Y
B.若Z的最高价氧化物遇Y的氢化物溶液混合后有气体放出,则W的氢化物不稳定
C.若Y、W的质子数之和为23,则Z能形成碱性氧化物
D.若X能形成两种常见液态化合物,则W单质的溶液有漂白性
查看答案和解析>>
科目:高中化学 来源:2016届甘肃省高三上学期10月月考化学试卷(解析版) 题型:选择题
NA表示阿伏伽德罗常数的数值,下列说法不正确的是
A.将1molNH4NO3溶于一定浓度的稀氨水中,溶液呈中性,若不考虑挥发,溶液中一定含有NA个NH4+
B.1mol/LCH3COOH与1mol/L CH3COONa溶液等体积混合,溶液中CH3COOH和CH3COO-的总数为2NA
C.常温常压下,3.6g H2O中含有电子数为2NA
D.含有2NA个氧原子的氧气与臭氧的混合气体的质量为32g
查看答案和解析>>
科目:高中化学 来源:2015-2016学年江苏省泰州市姜堰区高二上学期期中选修化学试卷(解析版) 题型:选择题
在容积固定的容器中发生反应:A(g)+2B(g) 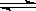 C (g) ΔH<0,各物质浓度如表所示:
C (g) ΔH<0,各物质浓度如表所示:
浓度 时间 | c(A)/mol·L-1 | c(B)/mol·L-1 | c(C)/mol·L-1 |
0 | 0.8 | 1.6 | 0 |
2 min | 0.6 | x | 0.2 |
4 min | 0.3 | 0.6 | 0.5 |
6 min | 0.3 | 0.6 | 0.5 |
下列说法错误的是
A.2~4 min内用B表示的平均反应速率为0.3 mol·L-1·min-1
B.反应在第2 min时改变了条件,可能是加入了催化剂
C.反应在第2 min时改变了条件,可能是增加了B的浓度
D.若加入催化剂,平衡时气体混合物的总物质的量保持不变
查看答案和解析>>
科目:高中化学 来源:2015-2016学年湖北省高二上第一次月考化学试卷(解析版) 题型:填空题
(8分)氢气是一种清洁能源,氢气的制取与储存是氢能源利用领域的研究热点。
已知:CH4(g)+ H2O(g)  CO(g)+3H2(g) Δ H =-206.2kJ·mol-1
CO(g)+3H2(g) Δ H =-206.2kJ·mol-1
CH4(g)+ CO2(g)  2CO(g)+2H2(g) ΔH =-247.4kJ·kJmol-1
2CO(g)+2H2(g) ΔH =-247.4kJ·kJmol-1
2H2S(g)  2H2(g)+S2(g) ΔH =+169.8kJ·kJmol-1
2H2(g)+S2(g) ΔH =+169.8kJ·kJmol-1
(1)以甲烷为原料制取氢气是工业上常用的制氢方法。CH4(g)与H2O(g)反应生成CO2(g)和H2(g)的热化学方程式为_____________________。
(2)H2S热分解制氢时,常向反应器中通入一定比例空气,使部分H2S燃烧,其目的是__________________________;燃烧生成的SO2与H2S进一步反应,生成物在常温下均非气体,写出该反应的化学方程式: _____________________。
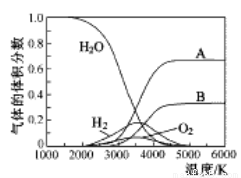
(3)H2O的热分解也可得到H2,高温下水分解体系中主要气体的体积分数与温度的关系如图所示。图中A、B表示的物质依次是______________。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年安徽省高一上学期第一次月考化学试卷(解析版) 题型:填空题
除去括号中的杂质,写出所加试剂的化学式,并写出相应的离子方程式:
(1)CaCl2(HCl)试剂: ,离子方程式:
(2)Cu(FeO)试剂: ,离子方程式:
(3)KNO3(KCl)①加入过量: ②再加入过量: ③过滤④加入适量的: ,蒸发结晶。(填试剂的化学式)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com