
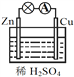
【题目】关于下图所示的原电池,下列说法正确的是 ( )
A. Zn片发生还原反应
B. 电子由锌片通过导线流向铜片
C. 该装置能将电能转化为化学能
D. 铜片上发生的反应为Cu - 2e- ![]() Cu2+
Cu2+
【答案】B
【解析】锌、铜和稀硫酸组成的原电池中,锌作负极,负极上锌失电子发生氧化反应;铜作正极,正极上氢离子得电子发生还原反应;电子从负极沿导线流向正极;原电池是化学能转化为电能的装置,以此分析。
A、锌、铜和稀硫酸组成的原电池中,锌作负极,负极上锌失电子发生氧化反应,选项A错误;B、锌、铜和稀硫酸组成的原电池中,锌作负极,铜作正极,电子从负极沿导线流向正极,即电子由锌片通过导线流向铜片,选项B正确;C、Zn、Cu、硫酸构成原电池,实现了化学能转化为电能,选项C错误;D、锌、铜和稀硫酸组成的原电池中,铜作正极,正极上氢离子得电子发生还原反应为2H++2e-=H2↑,溶液中没有铜离子,选项D错误;答案选D。


科目:高中化学 来源: 题型:
【题目】下列实验操作或事实与预期实验目的或所得结论对应正确的是( )
选项 | 实验操作或事实 | 实验目的或结论 |
A | 淡黄色试液 | 说明原溶液中一定含所有FeCl3 |
B | CaO | 用生石灰制备NaOH溶液 |
C | 新收集的酸雨 | 酸雨中一定含有SO42- |
D | H3PO3+2NaOH(足量)=Na2HPO3+2H2O | H3PO3属于三元酸 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于卤族元素的下列说法正确的是
A. 所有卤族元素的微粒都易得电子
B. 和氟同一主族的元素都是非金属元素
C. 化合物中卤族元素都显负价
D. 卤族元素原子的原子半径从上到下逐渐减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法一定正确的是 ( )
A. SO2的摩尔质量是64
B. 标准状况下,0.5 mol H2O所占体积约为11.2 L
C. 100 mL 0.1 mol/L NaOH溶液中含溶质的物质的量为0.01 mol
D. 标准状况下,11.2 L N2和CO的混合气体所含原子数约为3.01×1023
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有下列三种有机化合物:A.CH2=CH2 B.![]() C.CH3COOH
C.CH3COOH
(1)化合物C所含能电离出H+的原子团的名称是____________;
(2)三种化合物中能使溴的四氯化碳溶液褪色的是____________(填字母代号);
(3)写出在一定条件下,A发生聚合反应的化学方程式_______________
(4)写出在一定条件下,化合物C与CH3CH2OH发生反应的化学方程式__________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有下列五种物质:①CO2;②NH3;③SO2;④H2SO4;⑤NaCl。
(1)其中,能使品红溶液退色的是_____________(填序号,下同);
(2)属于电解质的是_____________ ;
(3)只含离子键的是________________;
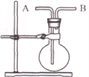
(4)利用下图装置并从B口进气,可收集的气体是___________ 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将CO2气体缓缓地通入含KOH、Ba(OH)2和KAlO2的混合溶液中直至过量,生成沉淀的物 质的量与所通CO2的体积关系如图所示。下列关于整个反应过程中的描述不正确的是
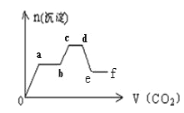
A. O~a段反应的化学方程式是Ba(OH)2+CO2![]() BaCO3↓+H2O
BaCO3↓+H2O
B. a~b段反应的离子方程式是2OH-+CO2![]() CO32-+H2O
CO32-+H2O
C. a~b段与c~d段所发生的反应相同
D. d~e段沉淀减少是由于碳酸钡固体溶解
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z均为短周期元素组成的物质,其转化关系如下:

请回答:
(1)若X为淡黄色固体,Z是单质。
①组成Z的元素在周期表中的位置是_____。
②取少量X与水反应,下列叙述正确的是_____(填字母)。
a.该反应是氧化还原反应
b.向反应后的溶液中滴加酚酞试剂,溶液变红
c.当有1 molX参加反应时,共转移2mol电子
(2)若X由两种元素组成,其中一种元素的最外层电子数比电子层数多3,另一种是地壳中含量最多的元素。Y与X的组成元素相同。
①X与水反应的化学方程式为_____。
②X与O2混合通入水中,恰好生成4molZ,则通入的X为____mol,O2为____mol。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com