
【题目】已知:反应CO(g)+H2O(g)![]() CO2(g)+H2(g)在不同的温度下的平衡常数分别为:
CO2(g)+H2(g)在不同的温度下的平衡常数分别为:
t/℃ | 700 | 800 | 830 | 1000 | 1200 |
k | 1.67 | 1.11 | 1.00 | 0.60 |
下列有关叙述不正确的是
A. 该反应平衡常数表达式为K=[c(CO2)·c(H2)]/[c(CO)·c(H2O)]
B. 该反应的逆反应是吸热反应
C. 830℃时,向恒容密闭容器中加入CO2 和H2各1mol,当测得CO2 的物质的量为0.4mol时,反应处于平衡状态
D. 若某温度下该反应中各物质的平衡浓度符合关系式:[c(CO2)/3c(CO)]=[c(H2O)/5c(H2)],则该温度是1000 C
【答案】C
【解析】
K是平衡常数,即一定温度下,可逆反应达平衡时,生成物浓度幂的乘积与反应物浓度幂的乘积之比,A正确;温度升高,K减少,该反应的正反应是放热反应,逆反应为吸热反应,B正确;设容器的体积为1L,830℃时,平衡常数为K=1;各量变化如下:
CO(g)+H2O(g)![]() CO2(g)+H2(g)
CO2(g)+H2(g)
起始量 1 1 0 0
变化量 0.4 0.4 0.4 0.4
某一时刻剩余量 0.6 0.6 0.4 0.4
带入浓度商计算:QC=[c(CO2)·c(H2)]/[c(CO)·c(H2O)]= (0.4×0.4)÷(0.6×0.6)=0.44<1,
反应未达平衡状态,C错误;[c(CO2)/3c(CO)]=[c(H2O)/5c(H2)],整理得:[c(CO2)·c(H2)]/[c(CO)·c(H2O)]=3/5=0.6=K, 对应温度为1000℃,D正确;正确选项C。


科目:高中化学 来源: 题型:
【题目】常温下,甲、乙两杯醋酸稀溶液,甲的pH=a,乙的pH=a+1,对下列叙述的判断正确的是
A. 物质的量浓度c (甲)>10c(乙)
B. 甲中水电离出来的H+的物质的量浓度是乙中水电离出来的H+的物质的量浓度的10倍
C. 中和等物质的量的NaOH溶液需甲、乙两杯醋酸溶液的体积,V(甲)=10V(乙)
D. 甲中的c (OH-)为乙中的c (OH-)的10倍
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知断裂1 mol C—H键,要吸收热量414.4 kJ;断裂1 mol C—C键,要吸收热量347.4 kJ;生成1 mol C===C键,会放出热量615.3 kJ;生成1 mol H—H键,会放出热量435.3 kJ,某有机物分解的反应可表示为:

若在反应中消耗了1 mol乙烷(反应物),则有关该反应的说法正确的是( )
A. 该反应放出251.2 kJ的热量 B. 该反应吸收251.2 kJ的热量
C. 该反应放出125.6 kJ的热量 D. 该反应吸收125.6 kJ的热量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】把足量熟石灰放入蒸馏水中,一段时间后达到平衡:Ca(OH)2(s)![]() Ca2+(aq)+
Ca2+(aq)+
2OH-(aq),下列叙述正确的是( )
A. 给溶液加热,溶液的pH升高
B. 恒温下向溶液中加入CaO,溶液的pH升高
C. 向溶液中加入Na2CO3溶液,则其中的Ca(OH)2的固体增多
D. 向溶液中加入少量的NaOH固体,则其中的Ca(OH)2的固体增多
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列溶液中微粒的物质的量浓度关系正确的是
A. 已知酸性![]() ,物质的量浓度相等的NaF与
,物质的量浓度相等的NaF与![]() 溶液中:c
溶液中:c![]()
B. 0.lmol·L-1的NaHX溶液pH为4,该溶液中: ![]()
C. 氯水中: ![]()
D. 25°C时,pH=8的![]() 溶液中,
溶液中,![]() 约为10-6mol·L-1
约为10-6mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】取100.0 mLNa2CO3和Na2SO4的混合溶液,加入过量BaCl2溶液后得到16.84g沉淀,用过量稀硝酸处理后沉淀质量减少至6.99g,同时溶液中有气泡产生。试求:
(1)原混合液中Na2SO4的物质的量浓度为_____;
(2)产生的气体在标准状况下的体积为多少__________?(要求写出计算过程,只写结果不给分)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列事实中,不能用勒夏特列原理解释的是
A. 合成氨工厂选择500℃的高温
B. 常温时,AgCl 在饱和氯化钠溶液中的溶解度小于在水中的溶解度
C. 热的纯碱溶液去油污效果更好
D. 开启啤酒瓶后,瓶中马上泛起大量泡沫
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示是组成细胞的主要元素及其比例,根据图所示信息回答下列问题:
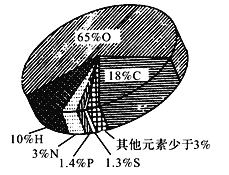
(1)构成细胞的主要元素有________。
(2)组成生物体的最基本元素占细胞鲜重的___________。
(3)硫元素主要存在于有机化合物的种类是___________。
(4)碳的含量没有氧多,为什么是最基本元素?_________________________________。
(5)C、H、N三种化学元素在干细胞中所占比例较高,而这三种元素在组成岩石圈的化学成分中,质量分数还不到1%,这个事实说明了______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表是关于有机物甲、乙的信息:

根据表中信息回答下列问题:
(1)甲与溴的四氯化碳溶液反应的化学方程式:________;
(2)写出一定条件下甲发生聚合反应的化学方程式:_______________________。
(3)甲的同系物用通式CnHm表示,乙的同系物用通式CxHy表示,当CnHm、CxHy分别出现同分异构体时,碳原子数的最小值n=________,x=________。
(4)乙具有的性质是________(填编号)。
①无色无味液体 ②有毒 ③不溶于水 ④密度比水大 ⑤能使酸性KMnO4溶液和溴水褪色 ⑥任何条件下均不与氢气反应 ⑦与溴水混合后液体分层且上层呈橙红色
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com