
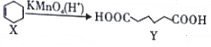 £¬ĻĀĮŠĖµ·Ø“ķĪóµÄŹĒ£Ø””””£©
£¬ĻĀĮŠĖµ·Ø“ķĪóµÄŹĒ£Ø””””£©| A£® | X·Ö×ÓÖŠĖłÓŠĢ¼Ō×ÓŅ»¶ØŌŚĶ¬Ņ»Ę½ĆęÉĻ | |
| B£® | XÓėŅŅĻ©²»ŹōÓŚĶ¬ĻµĪļ | |
| C£® | YæÉ·¢ÉśČ”“ś·“Ó¦”¢Ńõ»Æ·“Ó¦ | |
| D£® | YµÄŗ¬ÓŠĻąĶ¬¹ŁÄÜĶŵÄĶ¬·ÖŅģ¹¹ĢåÓŠ8Ö֣ز»æ¼ĀĒĮ¢ĢåŅģ¹¹£© |
·ÖĪö A£®XÖŠŗ¬ÓŠŃĒ¼×»ł£¬¾ßÓŠ¼×Ķé½į¹¹ĢŲµć£»
B£®XĪŖ»·×“»ÆŗĻĪļ£¬ÓėŅŅĻ©½į¹¹²»Ķ¬£»
C£®YÖŠŗ¬ÓŠōČ»ł£¬¾ßÓŠōČĖįŠŌÖŹ£»
D£®Y½į¹¹¼ņŹ½ĪŖHOOC£ØCH2£©4COOH£¬-CH2CH2CH2CH2-µÄĶ¬·ÖŅģ¹¹ĢåÓŠ8ÖÖ£®
½ā“š ½ā£ŗA£®XÖŠŗ¬ÓŠŃĒ¼×»ł£¬¾ßÓŠ¼×Ķé½į¹¹ĢŲµć£¬ĖłŅŌĖłÓŠCŌ×Ó²»æÉÄܹ²Ę½Ćę£¬¹ŹA“ķĪó£»
B£®XĪŖ»·×“»ÆŗĻĪļ£¬ÓėŅŅĻ©½į¹¹²»Ķ¬£¬Ōņ²»ŹĒĶ¬ĻµĪļ£¬¹ŹBÕżČ·£»
C£®YÖŠŗ¬ÓŠōČ»ł£¬¾ßÓŠōČĖįŠŌÖŹ£¬ÄÜŗĶ¼ī·¢ÉśÖŠŗĶ·“Ó¦£¬ŹōÓŚÓŠ»śĪļÄÜČ¼ÉÕ¶ų·¢ÉśŃõ»Æ·“Ó¦£¬¹ŹCÕżČ·£»
D£®Y½į¹¹¼ņŹ½ĪŖHOOC£ØCH2£©4COOH£¬-CH2CH2CH2CH2-µÄĶ¬·ÖŅģ¹¹ĢåÓŠ8ÖÖ£¬Į½øöōČ»łŌŚĶ¬Ņ»øöĢ¼Ō×ÓÉĻŗ¬ÓŠ2ÖÖ£¬ŌŚ²»Ķ¬Ģ¼Ō×ÓÉĻŗ¬ÓŠ6ÖÖ£¬ĖłŅŌ·ūŗĻĢõ¼žµÄŅ»¹²8ÖÖ£¬¹ŹDÕżČ·£»
¹ŹŃ”A£®
µćĘĄ ±¾Ģāæ¼²éÓŠ»śĪļ½į¹¹ŗĶŠŌÖŹ£¬ĪŖøßĘµæ¼µć£¬²ąÖŲæ¼²éѧɜµÄ·ÖĪöÄÜĮ¦£¬Ć÷Č·¹ŁÄÜĶż°ĘäŠŌÖŹ¹ŲĻµŹĒ½ā±¾Ģā¹Ų¼ü£¬²ąÖŲæ¼²éĻ©Ģž”¢ōČĖįŠŌÖŹ£¬ŅדķŃ”ĻīŹĒD£¬ŗܶąĶ¬Ń§ĶłĶłĀ©µōĮ½øöōČ»łŌŚĶ¬Ņ»øöĢ¼Ō×ÓÉĻ¶ųµ¼ÖĀ“ķĪó£¬ĢāÄæÄŃ¶Č²»“ó£®


 ѧʌø“Ļ°Ņ»±¾ĶØѧĻ°×ܶÆŌ±ĘŚÄ©¼ÓŹī¼ŁŃÓ±ßČĖĆń³ö°ęÉēĻµĮŠ“š°ø
ѧʌø“Ļ°Ņ»±¾ĶØѧĻ°×ܶÆŌ±ĘŚÄ©¼ÓŹī¼ŁŃÓ±ßČĖĆń³ö°ęÉēĻµĮŠ“š°ø Ć¢¹ū½ĢøØŹī¼ŁĢģµŲÖŲĒģ³ö°ęÉēĻµĮŠ“š°ø
Ć¢¹ū½ĢøØŹī¼ŁĢģµŲÖŲĒģ³ö°ęÉēĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ĀČ»ÆÄĘÓėÅØĮņĖį»ģŗĻ¼ÓČČ£ŗH2SO4£ØÅØ£©+2Cl-$\frac{\underline{\;\;”÷\;\;}}{\;}$SO${\;}_{4}^{2-}$+2HCl”ü | |
| B£® | ¹żĮæµÄĮņ»ÆÄĘČÜŅŗÓėĀČ»ÆĢśČÜŅŗ·“Ó¦£ŗ2Fe3++S2-ØT2Fe2++S”ż | |
| C£® | Ģ¼ĖįĒāļ§ČÜŅŗÓė×ćĮæNaOHČÜŅŗ»ģŗĻŗó¼ÓČČ£ŗNH${\;}_{4}^{+}$+HCO${\;}_{3}^{-}$+2OH-$\frac{\underline{\;\;”÷\;\;}}{\;}$CO${\;}_{3}^{2-}$+NH3”ü+2H2O | |
| D£® | Ļņ“ĪĀČĖįøĘČÜŅŗÖŠĶØČėÉŁĮæSO2£ŗCa2++2ClO-+SO2+H2OØTCaSO3”ż+2HClO |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ŌŚÕįĢĒÖŠ¼ÓČėÅØĮņĖįŗó³öĻÖ·¢ŗŚµÄĻÖĻó£¬ĖµĆ÷ÅØĮņĖį¾ßÓŠĶŃĖ®ŠŌ | |
| B£® | NaµÄ½šŹō»ī¶ÆŠŌ±ČMgĒ棬ĖµĆ÷æÉÓĆNaÓėMgCl2ČÜŅŗ·“Ó¦ÖĘMg | |
| C£® | ³£ĪĀĻĀ£¬ÅØĻõĖįæÉŅŌÓĆĀĮ¹ŽÖü“ę£¬ĖµĆ÷ĀĮÓėÅØĻõĖį·“Ӧɜ³ÉĮĖÖĀĆܵÄŃõ»ÆĪļ | |
| D£® | ĻņµāĖ®ÖŠµĪ¼ÓCCl4£¬Õńµ“¾²ÖĆŗó·Ö²ć£¬ĻĀ²ć³Ź×ĻŗģÉ«£¬ĖµĆ÷æÉÓĆCCl4“ÓµāĖ®ÖŠŻĶČ”µā |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŹµŃéĢā
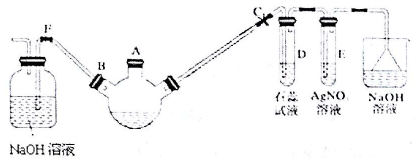
 £®
£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 1£ŗ5 | B£® | 1£ŗ4 | C£® | 3£ŗ2 | D£® | 5£ŗ1 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
| ŹµŃé²½Öč | Ō¤ĘŚµÄŹµŃéĻÖĻóŗĶ½įĀŪ |
| ²½Öč£ŗČ”Ņ»¶ØĮæµÄ¹ĢĢå²śĪļÓŚŹŌ¹ÜÖŠ£¬¼ÓČėŹŹĮæÕōĮóĖ®½ųŠŠČܽā£¬Č»ŗóĶłŹŌ¹ÜÖŠ¼ÓČėŹŹĮæµÄ CuCl2ČÜŅŗ²¢¹żĀĖ£® | \ |
| ²½Öč2£ŗ Č”1µÄĀĖŅŗ¼ÓČė·ÓĢŖŹŌŅŗ£¬ČōČÜŅŗ±äŗģ£¬ | ĖµĆ÷ÓŠNaOH |
| ²½Öč3£ŗ Č”1µÄĀĖŅŗ¼ÓČėBaCl2ČÜŅŗ£¬Čō²śÉś°×É«³Įµķ£¬ | ĖµĆ÷ÓŠNa2SO4 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ¶ąŃ”Ģā
| A£® | ÖĘĀČŅŅĶé£ŗCH2=CH2+HCl$”ś_{”÷}^{“߻ƼĮ}$CH3CH2Cl | |
| B£® | ÖĘ¼×»ł±ūĻ©Ėį¼×õ„£ŗCH3C”ŌCH+CO+CH3OH $\stackrel{Pd}{”ś}$ CH2=C£ØCH3£©COOCH3 | |
| C£® | ÖĘCuSO4£ŗ2Cu+O2=2CuO£¬CuO+H2SO4£ØĻ”£©ØTCuSO4+H2O | |
| D£® | ÖĘCu£ØNO3£©2£ŗCu+4HNO3£ØÅØ£©ØTCu£ØNO3£©2+2NO2”ü+2H2O |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
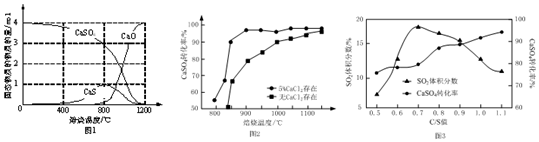
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 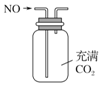 ÓĆĶ¼ĖłŹ¾×°ÖĆ£ØÕż·Å£©æÉŹÕ¼ÆNOĘųĢå | |
| B£® | 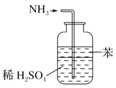 ÓĆĶ¼ĖłŹ¾×°ÖĆæÉĪüŹÕ¶ąÓą°±ĘųĒŅÄÜ·ĄÖ¹µ¹Īü | |
| C£® | 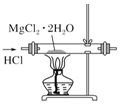 ÓĆ×°ÖĆÖĘČ”ĪŽĖ®MgCl2 | |
| D£® | 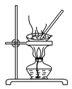 ÓĆ×°ÖĆÕōøÉNH4Cl±„ŗĶČÜŅŗ»ńČ”NH4Cl¾§Ģå |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com