
 和
和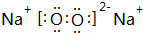 ;
; ;
;分析 根据原子半径D>C>A>B,且A、B同周期,A、C同主族,推知A、B、C、D在周期表中的大致相对位置为: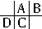 ,C的原子核内的质子数等于A、B原子核内的质子数之和,C质子数等于A+8,故B为8号元素氧.因A、C为主族元素,且C最外层电子数为D的4倍,则D最外层电子数只能为1,故D为钠,C为硅,A为碳,据此解答.
,C的原子核内的质子数等于A、B原子核内的质子数之和,C质子数等于A+8,故B为8号元素氧.因A、C为主族元素,且C最外层电子数为D的4倍,则D最外层电子数只能为1,故D为钠,C为硅,A为碳,据此解答.
解答 解:根据原子半径D>C>A>B,且A、B同周期,A、C同主族,推知A、B、C、D在周期表中的大致相对位置为: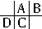 ,C的原子核内的质子数等于A、B原子核内的质子数之和,C质子数等于A+8,故B为8号元素氧.因A、C为主族元素,且C最外层电子数为D的4倍,则D最外层电子数只能为1,故D为钠,C为硅,A为碳.
,C的原子核内的质子数等于A、B原子核内的质子数之和,C质子数等于A+8,故B为8号元素氧.因A、C为主族元素,且C最外层电子数为D的4倍,则D最外层电子数只能为1,故D为钠,C为硅,A为碳.
(1)B与D形成的化合物为Na2O、Na2O2,电子式分别为: 、
、 ,
,
故答案为: ;
; ;
;
(2)用电子式表示CO2的形成过程: ,故答案为:
,故答案为: ;
;
(3)A、B、D组成的化合物为Na2CO3,B、C组成的化合物为SiO2,二者相互反应的化学方程式:SiO2+Na2CO3$\frac{\underline{\;高温\;}}{\;}$Na2SiO3+CO2↑,
故答案为:SiO2+Na2CO3$\frac{\underline{\;高温\;}}{\;}$Na2SiO3+CO2↑.
点评 本题考查元素位置结构性质的关系应用,题目难度中等,本题的关键是正确推断元素的种类,确定其在周期表中的相对位置.


科目:高中化学 来源: 题型:选择题
| A. | C6H12O6(葡萄糖)+6O2═6CO2+6H2O | B. | CH3COOH+KOH═CH3COOK+H2O | ||
| C. | 所有高温条件下发生的反应 | D. | C+CO2$\frac{\underline{\;\;△\;\;}}{\;}$2CO |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Al3+、NH4+、Cl-、CO32- | B. | Na+、CH3COO-、K+、HCO3- | ||
| C. | Fe2+、Cl-、Na+、NO3- | D. | K+、I-、CO3-、Na+ |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
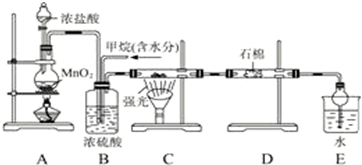
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
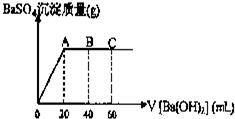 已知在某温度T℃时,某稀硫酸和盐酸混合液中,c(H+)=10-amol•L-1,c(OH-)=10-bmol•L-1,已知a+b=12.向20mL该混合酸溶液中逐滴加入pH=11Ba(OH)2溶液,生成BaSO4的质量与加入的Ba(OH)2溶液体积关系如图所示,当加入60mL Ba(OH)2溶液时,C点溶液的pH=6(体积变化忽略不计),试计算:
已知在某温度T℃时,某稀硫酸和盐酸混合液中,c(H+)=10-amol•L-1,c(OH-)=10-bmol•L-1,已知a+b=12.向20mL该混合酸溶液中逐滴加入pH=11Ba(OH)2溶液,生成BaSO4的质量与加入的Ba(OH)2溶液体积关系如图所示,当加入60mL Ba(OH)2溶液时,C点溶液的pH=6(体积变化忽略不计),试计算:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
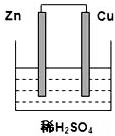 根据如图所示的装置,完成下列各空.
根据如图所示的装置,完成下列各空.查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | C作还原剂 | B. | CO2作氧化剂 | ||
| C. | 氧元素化合价降低 | D. | 氧元素化合价升高 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com