
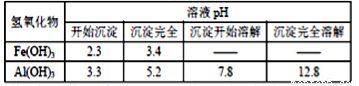
已知:Fe(OH)3和Al(OH)3沉淀的生成与溶解的量如下表。
向FeCl3、Al2(SO4)3的混合溶液中逐有加入Ba(OH)2溶液,形成沉淀的情况如下图所示.以下推断错误的是
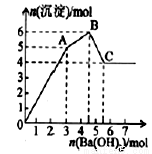
A.AB段可能发生的反应:2Ba2++3OH-+2SO42-+Al3+=2BaSO4↓+Al(OH)3↓
B.C点对应的沉淀:Fe(OH)3和BaSO4
C.OA段可能发生的反应:3Ba2++6OH-+3SO42-+Al3++Fe3+=3BaSO4↓+Fe(OH)3↓+Al(OH)3↓
D.据图计算原溶液中:c(Cl-)=c(SO42-)
科目:高中化学 来源: 题型:选择题
 常温下,取20mL某浓度的HCl作为待测液,用一定物质的量浓度的NaOH溶液进行滴定(假设盐酸与NaOH溶液混合后体积变化忽略不计),滴定过程中溶液的pH变化如图所示.下列叙述正确的是( )
常温下,取20mL某浓度的HCl作为待测液,用一定物质的量浓度的NaOH溶液进行滴定(假设盐酸与NaOH溶液混合后体积变化忽略不计),滴定过程中溶液的pH变化如图所示.下列叙述正确的是( )| A. | 所用HCl的浓度是0.09mol•L─1,NaOH溶液浓度为0.03mol•L-1 | |
| B. | 在B点,溶液中离子浓度关系为:c(Na+)>c(Cl-)>c(H+)>c(OH-) | |
| C. | A.B.C三点水的电离程度大小依次为:A>B>C | |
| D. | 滴定前,锥形瓶用待测液润洗,导致HCl浓度偏低 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.1mol•L-1的(NH4)2SO4溶液中:c(NH4+)>c(SO42-)>c(H+)>c(OH-) | |
| B. | 0.1 mol•L-1 NaHS溶液中:c(H2S)+c(H+)=c(OH-)+c(S2-) | |
| C. | 将pH=2的盐酸和pH=12的氨水等体积混合后的溶液中:c(NH4+)>c(Cl-)>c(OH-)>c(H+) | |
| D. | 0.1 mol•L-1 NH4HSO4溶液与0.1 mol•L-1 NaOH溶液等体积混合后的溶液中:c(Na+)>c(NH4+)>c(SO42-) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
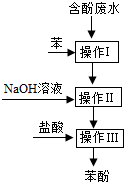
| A. | 操作I中苯作萃取剂 | |
| B. | 苯酚钠在苯中的溶解度比在水中的大 | |
| C. | 通过操作II苯可循环使用 | |
| D. | 三步操作均需要分液漏斗 |
查看答案和解析>>
科目:高中化学 来源:2017届湖南省长沙市高三上学期第三次月考模拟化学试卷 题型:选择题
一定温度下,在甲、乙、丙、丁四个恒容密闭容器中投入SO2(g)和O2(g),进行反应,2SO2(g)+O2(g) 2SO3(g),其起始物质的量及SO2的平衡转化率如下表所示。下列判断中正确的是
2SO3(g),其起始物质的量及SO2的平衡转化率如下表所示。下列判断中正确的是

A.甲中反应的平衡常数小于乙B.该温度下,该反应的平衡常数K为400
C.SO2的平衡转化率:a1>a2=a3D.容器中S03的物质的量浓度:丙=丁<甲
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 第一电离能:Al<Mg | B. | 共价键极性:H-F<H-Cl | ||
| C. | 硬度:Al2O3<NaCl | D. | 酸性:H2SO4>H2SO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙烯(乙炔):将气体通过盛KMnO4溶液的洗气瓶 | |
| B. | 溴乙烷(溴):加入CCl4,振荡,静置,分液 | |
| C. | 苯(苯酚):加足量NaOH溶液,振荡,静置,分液 | |
| D. | 乙醛(乙酸乙酯):加入NaOH溶液,振荡,静置,分液 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 ,属于共价(“离子”或“共价”)化合物.
,属于共价(“离子”或“共价”)化合物.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com