
��֪A��B��C��D�����ֳ������ʣ����ӦԪ�ص�ԭ������������������B��D���ڳ���������J��һ�ֺ�ɫ���壬I��Ũ��Һ���л�ԭ�ԣ�A��I��Ϊ��ѧ��ѧ�������ʣ�����֮���ת����ϵ����ͼ��ʾ��������������ͷ�Ӧ��������ȥ��
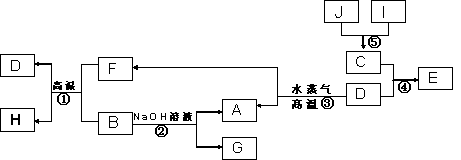
��ش��������⣺
(1) д���������D��Ԫ�������ڱ��е�λ�ã�___________________��
(2) ��д����Ӧ�ٵĻ�ѧ����ʽ��______________________________��
����E�ı�����Һ�����Ƶý��壬�û�ѧ����ʽ��ʾ�ù��̵�ԭ����_________________________��
(3) ��֪G��ˮ��Һ�Լ��ԣ���ԭ���ǣ������ӷ���ʽ��ʾ��_________��
(4) J��H2O2�ֽⷴӦ������������������J�����ữ��H2O2��Һ�У�J�ܽ���������+2�����ӣ��÷�Ӧ�����ӷ���ʽ��___________________ ��
 ��Կ���Ծ�ϵ�д�
��Կ���Ծ�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
������A��N��H����Ԫ����ɣ�0.01mol A������CuO��ַ�Ӧ���ɺ�ɫ
Cu��ͬʱ��������0.36gˮ�ͱ�״���µ����Ϊ0.224L��N2��B����Na��H��Ԫ��
��ɵ����ӻ��������ˮ��Ӧ����H2����Ϊ�������������C����ɫ��ӦΪ��ɫ����
��������������Է�������Ϊ39����ˮ��Ӧ�����ɰ�����
��1��A�Ļ�ѧʽΪ ��A��CuO��Ӧ�Ļ�ѧ����ʽΪ ��
��2��B�ĵ���ʽΪ ��
��3��C�д��ڵĻ�ѧ�� ��C������ϡ���ᷴӦ�Ļ�ѧ����ʽΪ ��
��4����һ������Ļ�����NH4H�����������ϣ�����������δ���Ƶã���˵�����ܵ�ԭ��
��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
���й����л����������ȷ���� ��������
A���ױ�����������ԭ�Ӿ���ͬһ��ƽ����
B��ú��������Һ���������������仯���̣��ɱ�Ϊ�����Դ
C�������������£�CH3C18OOC2H5��ˮ�������CH3C18OOH��C2H5OH
D�����ۡ���Ȼ��֬�������ʶ�������Ȼ�߷��ӻ�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�������µ�˵������l6O�� l8O��ת������ͨ����ѧ��Ӧʵ�֣��������ƵĻ�����ʱ����ʻ�ɫ�����Ƿ����˻�ѧ��Ӧ���ۼ���������һ���ǽ����������ֻ��һ��Ԫ����ɵ�����һ���Ǵ������ʯī����ʯ��ת���ǻ�ѧ�仯���� 5424CrΪ����һ�ֺ��أ�����������Ϊ30. ����˵������ȷ����( )
A���٢ܢ� B���٢ۢ� C���ۢ� D���ڢۢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��֪��2CO(g)+O2(g)=2CO2(g) ��H= ��566 kJ•mol��1
Na2O2(s)+CO2(g) = Na2CO3(s)+1/2O2(g) ��H= ��226 kJ•mol��1
���б�����ȷ����(NA��������٤����������ֵ) ( )
A��1molCOȼ��ʱ�ų�������Ϊ283 kJ•mol��1
B��Na2O2(s)+CO(g) = Na2CO3(s) ��H= ��509 kJ•mol-1
C��Na2O2(s)��CO2(g)��Ӧ�ų�226 kJ����ʱ����ת����Ϊ2NA
D��Na2O2��Na2CO3���������Ӹ����Ȳ�ͬ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
���������У������������������һ������ʯ�ͻ�����չˮƽ���ǣ�������
A������ B����ϩ C���� D���Ҵ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
���Է�����ָ�ڷ��ӽṹ �У���a��b��c��dΪ�˴˻�����ͬ��ԭ�ӻ�ԭ����ʱ���ƴ˷���Ϊ���Է��ӣ�����̼ԭ��Ϊ����̼ԭ�ӡ����з�����ָ����̼ԭ�ӣ��á��ǣ���������̼ԭ�ӵ���
�У���a��b��c��dΪ�˴˻�����ͬ��ԭ�ӻ�ԭ����ʱ���ƴ˷���Ϊ���Է��ӣ�����̼ԭ��Ϊ����̼ԭ�ӡ����з�����ָ����̼ԭ�ӣ��á��ǣ���������̼ԭ�ӵ���
A������Ƭϩ B������
B������
C�����״�  D������
D������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�������ӷ���ʽ�������( )
A����Ba(OH)2��Һ�еμ�ϡ���Ba2����2OH����2H���� SO42 �� =BaSO4����2H2O
B��Cl2ͨ��NaOH��Һ��Cl2��2OHһ��Cl�D��ClO�D��H2O
C��AlCl3��Һ�м������ϡ��ˮ:Al3����4NH3��H2O��AlO�D 2��4NH��4��2H2O
D��Ǧ�����س��ʱ��������Ӧ��PbSO4�� 2H2O��2e- = PbO2��4H����SO42 ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
������������3�ְ����������ˮ�������ɵ����ĵĽṹ��ʽ��

�������ij���ˮ��ʱ�������ܲ����İ������ǣ� ��
A.  B.
B.
C. NH2��CH2��COOH D.
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com