
| A、蒸馏操作时,应使温度计水银球的上端与蒸馏烧瓶的支管口下端相平 |
| B、用玻璃棒蘸取Na2CO3溶液,滴在干燥的pH试纸上,测定该溶液的pH |
| C、用纯碱溶液洗涤黏附在试管壁上的油 |
| D、蒸发结晶时应将溶液蒸干后再停止加热 |


科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
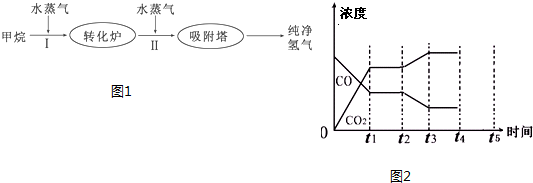
| 温度/℃ | 400 | 500 | 830 |
| 平衡常数K | 10 | 9 | 1 |
| 实验编号 | 反应物投入量 | 平衡时H2浓度 | 吸收或放出的热量 | 反应物转化率 |
| A | 1、1、0、0 | c1 | Q1 | α1 |
| B | 0、0、2、2 | c2 | Q2 | α2 |
| C | 2、2、0、0 | c3 | Q3 | α3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
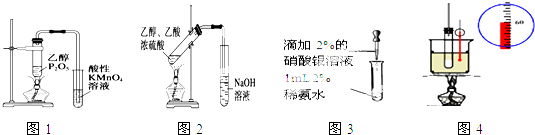
| A、图1可证明乙醇发生消去反应生成了乙烯 |
| B、图2用于实验室制备乙酸乙酯 |
| C、图3用于配制银氨溶液 |
| D、图4用于实验室制硝基苯 |
查看答案和解析>>
科目:高中化学 来源: 题型:
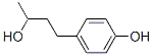 最近我国质检总局通报,日本佳丽宝公司生产的化妆品使用后皮肤会出现白斑,其中的有害成分为杜鹃醇(结构如图),有关杜鹃醇的说法不正确的是( )
最近我国质检总局通报,日本佳丽宝公司生产的化妆品使用后皮肤会出现白斑,其中的有害成分为杜鹃醇(结构如图),有关杜鹃醇的说法不正确的是( )| A、分子式为:C10H14O2 |
| B、水溶液酸性一定比碳酸强 |
| C、能与FeCl3溶液发生显色反应 |
| D、最多可与含3molBr2的溴水反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 相关实验 | 预期目的 | |
| A. | 在少量食用碱中滴加食醋 | 探究食用碱是碳酸钠还是碳酸氢钠 |
| B. | 在食用盐中滴加少量淀粉液 | 探究食用盐是否为加碘盐 |
| C. | 用激光笔照射淀粉液 | 探究淀粉液是胶体还是溶液 |
| D | 将鸡蛋白溶于水后,滴加AgNO3溶液 | 验证蛋白质中含有氯元素 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
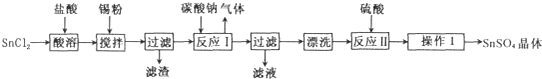
查看答案和解析>>
科目:高中化学 来源: 题型:
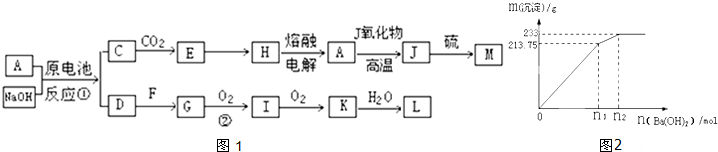
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、加入一定量pH=2的醋酸,混合后所得的溶液中:c(CH3COO-)+c(OH-)=c(NH4+)+c(H+) |
| B、向其中加入一定量的水,NH3?H2O的电离平衡正移,溶液中所有离子浓度均减小 |
| C、与等体积、pH=2的盐酸混合后所得的溶液中:c(Cl-)>c(NH4+)>c(H+)>c(OH-) |
| D、c(NH4+)+c(NH3?H2O)=1.0×10-12 mol?L-1 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com