
| A. | C3N4晶体是分子晶体 | |
| B. | C3N4晶体中,C原子采用sp3杂化,氮原子采用sp2杂化 | |
| C. | C3N4晶体中,C-N键的键长比金刚石中的C-C键的键长要短 | |
| D. | C3N4晶体中存在配位键 |
分析 A.金刚石为原子晶体,已知C3N4晶体具有和金刚石类似的结构,很可能具有比金刚石更大的硬度,据此作出判断;
B.每个原子周围要形成8电子稳定结构;
C.成键原子间核间距离为键长,键长和原子半径有关,碳和氮位于同一周期,根据半径变化规律作出判断;
D.形成配位键,需要一种原子提供空轨道,另一原子提供孤对电子.
解答 解:A.由信息可知,C3N4晶体很可能具有比金刚石还大的硬度,且原子间均以单键结合,所以C3N4为原子晶体,故A错误;
B.因为C的最外层有4个电子,每个电子与另一个N形成C-N(一对共用电子对),因此一个碳原子连接4个N原子,价层电子对数为4,为sp3杂化,因为N的最外层有5个电子,每个电子与另一个C形成N-C(一对共用电子对),因此一个N原子连接3个C原子,成键电子对为3,孤电子对数为1,价层电子数为4,为sp3杂化,故B错误;
C.因N的原子半径比C原子半径小,则C3N4晶体中,C-N键的键长比金刚石中C-C键的键长要短,故C正确;
D.C、N均满足最外层8电子稳定结构,没有空轨道,不符合形成配位键的条件,故D错误.
故选C.
点评 本题考查原子晶体的性质及作用力,明确信息是解答本题的关键,熟悉原子晶体的构成微粒、作用力、空间结构即可解答,题目难度不大,注重知识的迁移能力来分析解答.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 表述Ⅰ | 表述Ⅱ | |
| A | 在水中,NaCl的溶解度比I2的溶解度大 | NaCl晶体中C1-与Na+间的作用力大于碘晶体中分子间的作用力 |
| B | 通常条件下,CH4分子比PbH4分子稳定性高 | Pb的原子半径比C的大,Pb与H之间的键能比C与H间的小 |
| C | NaCl的熔点比MgO的熔点高 | NaCl的晶格能比MgO的晶格能大 |
| D | P4O10、C6H12O6溶于水后均不导电 | P4O10、C6H12O6均属于共价化合物 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
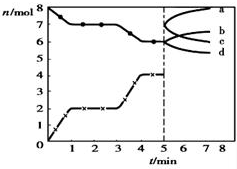
| A. | 1~3min时,v(CO)=v(CO2) | |
| B. | 当容器内的压强不变时,该反应一定达到平衡状态,且$\frac{P(平衡)}{P(开始)}<1$ | |
| C. | 若3min时温度由T1升高到T2,则Q>O,且$\frac{K({T}_{2})}{K({T}_{1})}$=4.7 | |
| D. | 5min时再充入一定量的CO,c、b曲线分别表示n(CO)、n(CO2)的变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 水在结冰时体积膨胀,是由于水分子之间存在氢键 | |
| B. | 由于N、O、F的第一电离能较大,所以NH3、H2O、HF分子间可以形成氢键 | |
| C. | 只要有氢键,物质的熔点和沸点就会升高 | |
| D. | H2O是一种非常稳定的化合物,这是由于氢键所致 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
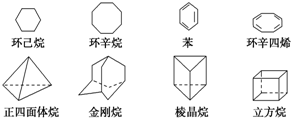 下列是八种环状的烃类物质:
下列是八种环状的烃类物质:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 只有①②③⑤ | B. | 只有①④⑤ | C. | 只有①③④⑤ | D. | 全部 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com