
【题目】下列说法正确的是
A.分子中含有两个氢原子的酸一定是二元酸
B.“血液透析”利用了胶体的性质
C.Na2O、Na2O2组成元素相同,与CO2反应产物相同
D.酸酐一定是氧化物,金属氧化物一定是碱性氧化物
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.正反应是放热反应的可逆反应,升高温度v(正)>v(逆)
B.加压可使速率加快,是因为增加活化分子百分数而使反应速率加快
C.活化分子的碰撞不一定都能发生化学反应
D.催化剂可改变反应进程,故加催化剂改变了一个反应的 △H
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在配制一定物质的量浓度的盐酸时,下列错误操作可使所配制溶液浓度偏高的是
A.溶解搅拌时有液体飞溅
B.用量筒量取浓盐酸时仰视读数
C.定容时仰视容量瓶瓶颈刻度线
D.定容摇匀后见液面下降,再加水至刻度线
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,将NH4NO3溶于水得无色溶液,为使该溶液中的c(NH4+)∶c(NO3-)=1∶1,可以采取的下列措施是
A.加入适量的HNO3,抑制NH4+水解 B.加入适量的氨水,使溶液的pH等于7
C.加入适量的NH4NO3(s) D.加入适量的NaOH,使溶液的pH等于7
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列对“改变反应条件,导致化学反应速率改变”的原因描述不正确的是
A.增大反应物的浓度,活化分子百分数增加,反应速率加快
B.增大气体反应体系的压强,单位体积中活化分子数增多,气体反应速率加快
C.升高反应的温度,活化分子百分数增加,有效碰撞的几率提高,反应速率增大
D.催化剂通过改变反应路径,使反应所需的活化能降低,反应速率增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】煤化工中常需研究不同温度下平衡常数、投料比及产率等问题。
已知:CO(g)+H2O(g)![]() H2(g)+CO2(g)的平衡常数随温度的变化如下表:
H2(g)+CO2(g)的平衡常数随温度的变化如下表:

试回答下列问题:
(1)上述反应平衡常数的表达式为_____________,正反应是___________反应(填“放热”或“吸热”)。
(2)某温度下,上述反应达到平衡后,保持容器体积不变升高温度,正反应速率_________(填“增大”“减小”或“不变”),容器内混合气体的压强______________(填“增大”“减小”或“不变”)。
(3)830 ℃时,在恒容反应器中发生上述反应,按下表中的物质的量投入反应混合物,其中向正反应方向进行的有______________(选填字母)。
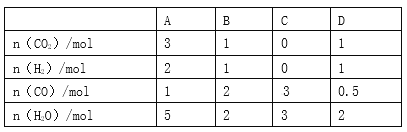
(4)830 ℃时,在2 L的密闭容器中加入4 mol CO(g)和6 mol H2O(g)达到平衡时,CO的转化率是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】纳米级Cu2O由于具有优良的催化性能而受到关注。已知:
①2Cu(s)+![]() O2(g)===Cu2O(s) ΔH=-169 kJ·mol-1,
O2(g)===Cu2O(s) ΔH=-169 kJ·mol-1,
②C(s)+![]() O2===CO(g) ΔH=-110.5 kJ·mol-1,
O2===CO(g) ΔH=-110.5 kJ·mol-1,
③2Cu(s)+ O2(g)===2CuO(s) ΔH=-314 kJ·mol-1
(1)则工业上用炭粉在高温条件下还原CuO制取Cu2O和CO的热化学方程式为______________________。
(2)某兴趣小组的同学用下图所示装置研究有关电化学的问题(甲、乙、丙三池中溶质足量),当闭合该装置的电键K时,观察到电流计的指针发生了偏转。

请回答下列问题:
①甲池为__________(填“原电池”“电解池”或 “电镀池”),A电极的电极反应式为______________
②丙池中电池总反应的离子方程式:_______________________
③当乙池中C极质量减轻10.8 g时,甲池中B电极理论上消耗O2的体积为______mL(标准状况)。
④一段时间后,断开电键K,下列物质能使乙池恢复到反应前浓度的是________(填选项字母)。
A.CuO B. Cu C.Cu(OH)2 D.Cu2(OH)2CO3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求填空:
(1)0.2molO3和0.3molO2的质量___________(选填“相等”、“不相等”或“无法判断”),分子数之比为__________,所含原子数之比为___________,在相同条件下的体积之比为_____________。
(2)73gHCl气体中含有_____________个分子,标准状况下占有的体积为_____________L。
(3)相同物质的量浓度的KCl、MgCl2、AlCl3三种溶液,分别与AgNO3溶液反应,当生成的AgCl的沉淀的质量之比为3:2:1时,三种溶液的体积比为__________。
(4)标准状况下VL氯化氢气体溶解在1L水中,所得溶液的密度为ρgmL,溶液中溶质的质量分数为ω,物质的量浓度为cmolL-1,则ω=__________(任写一种表达式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列分离物质的方法不正确的是( )
A. 用蒸发结晶的方法分离碳酸钠和水
B. 用过滤的方法分离植物油和水
C. 用蒸馏的方法分离酒精和水
D. 用萃取和分液的方法用CCl4从碘水中提取碘
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com