
以某菱锰矿(含MnCO3、SiO2、FeCO3和少量Al2O3等)为原料通过以下方法可获得碳酸锰粗产品。
(已知:Ksp(MnCO3)=2.2×10-11,Ksp[Mn(OH)2]=1.9×10-13,Ksp[Al(OH)3]=1.3×10-33,Ksp[Fe(OH)3]=4.0×10-38)
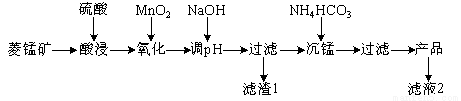
(1)滤渣1中,含铁元素的物质主要是 (填化学式,下同);加NaOH调节溶液的pH约为5,如果pH过大,可能导致滤渣1中 含量减少。
(2)滤液2中,+1价阳离子除了H+外还有 (填离子符号)。
(3)取“沉锰”前溶液a mL于锥形瓶中,加入少量AgNO3溶液(作催化剂)和过量的1.5%(NH4)2S2O8溶液,加热,Mn2+被氧化为MnO,反应一段时间后再煮沸5 min[除去过量的(NH4)2S2O8],冷却至室温。选用适宜的指示剂,用b mol·L-1的(NH4)2Fe(SO4)2标准溶液滴定至终点,消耗(NH4)2Fe(SO4)2标准溶液V mL。
①Mn2+与(NH4)2S2O8反应的还原产物为 (填化学式)。
②“沉锰”前溶液中c(Mn2+)= mol·L-1。
(4)其他条件不变,“沉锰”过程中锰元素回收率与NH4HCO3初始浓度(c0)、反应时间的关系如下图所示。

①NH4HCO3初始浓度越大,锰元素回收率越 (填“高”或“低”),简述原因 。
②若溶液中c(Mn2+)=1.0 mol·L-1,加入等体积1.8 mol·L-1 NH4HCO3溶液进行反应,计算20~40 min内v(Mn2+)= 。
科目:高中化学 来源:2015-2016学年河北省冀州市高一下期末化学试卷(解析版) 题型:选择题
下表是部分短周期元素的原子半径及主要化合价,根据表中信息,判断以下叙述正确的是( )

A.L2+、R2-的核外电子数相等
B.单质与浓度相等的稀盐酸反应的速率为Q>L
C.氢化物的稳定性:H2T<H2R
D.M与T形成的化合物既能与强酸反应又能与强碱反应
查看答案和解析>>
科目:高中化学 来源:2015-2016学年四川省高一下第二次段考化学卷(解析版) 题型:选择题
关于如图所示的原电池,下列说法不正确的是

A.锌片发生氧化反应
B.电子由锌片通过导线流向铜片
C.铜片上反应式为Cu2++2e﹣═Cu
D.该电池的反应本质是氧化还原反应
查看答案和解析>>
科目:高中化学 来源:2016届江苏省等三校高三第四次模拟化学试卷(解析版) 题型:选择题
下列化学反应的离子方程式正确的是
A.Ba(OH)2溶液中滴加NH4HSO4溶液至Ba2+沉淀完全:Ba2++OH-+H++SO42-=BaSO4↓+H2O
B.将过量SO2气体通入氨水中:SO2 + NH3·H2O =NH4++ HSO3-
C.用醋酸除去水垢中的CaCO3 : CaCO3 + 2 H+=Ca2++ H2O+CO2↑
D.用KIO3氧化酸性溶液中的KI: 5I-+IO3- +3H2O=3I2+6OH-
查看答案和解析>>
科目:高中化学 来源:2016届江苏省等三校高三第四次模拟化学试卷(解析版) 题型:选择题
化学学科需要借助化学语言来描述。下列化学用语正确的是
A.甲烷分子的球棍模型: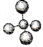
B.NH4Br的电子式:
C.氯原子的结构示意图: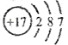
D.邻羟基苯甲酸的结构简式: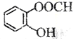
查看答案和解析>>
科目:高中化学 来源:2016届湖北省高三5月模拟四理综化学试卷(解析版) 题型:选择题
下图是一种蓄电池的示意图。被膜隔开的电解质分别为Na2S2和NaBr3,放电后变为Na2S4和NaBr。已知放电时Na+ 由乙池向甲池移动。下面对该装置工作过程中叙述正确的是
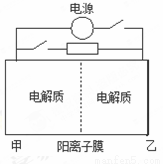
A.放电过程,甲池发生氧化反应
B.放电过程,电池反应:2S22-+ Br3-= S42-+ 3Br-
C.充电过程,乙池为阳极室
D.充电过程,当阳极室阴离子增加2mol,整个电路中电子转移2mol
查看答案和解析>>
科目:高中化学 来源:2016届湖北省高三5月模拟三理综化学试卷(解析版) 题型:实验题
为回收利用废钒催化剂(含有V2O5、VOSO4及不溶性残渣),科研人员最新研制了一种离子交换法回收钒的新工艺,主要流程如下:

部分含钒物质在水中的溶解性如下:
物质 | VOSO4 | V2O5 | NH4VO3 | (VO2)2SO4 |
溶解性 | 可溶 | 难溶 | 难溶 | 易溶 |
回答下列问题:
(1)工业由V2O5冶炼金属钒常用铝热剂法,写出该反应的化学方程式 .
(2)图中所示滤液中含钒的主要成分为 (写化学式).
有学者建议将滤液进行如下处理后再用KClO3氧化

上图中的萃取与反萃取的变化过程可简化为(下式R表示VO2+,HA表示有机萃取剂).
RSO4(水层)+ 2HA(有机层) RA2(有机层)+H2SO4(水层),上图中的X试剂为 _____;这种萃取与反萃取过程有别于用CCl4萃取碘水中的碘,二者的相同点是__________________,不同点是_______________
RA2(有机层)+H2SO4(水层),上图中的X试剂为 _____;这种萃取与反萃取过程有别于用CCl4萃取碘水中的碘,二者的相同点是__________________,不同点是_______________
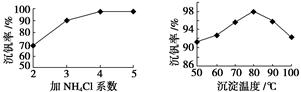
(3)该工艺中反应③的沉淀率(又称沉钒率)是回收钒的关键之一,该步反应的离子方程式_____________ ;沉钒率的高低除受溶液pH影响外,还需要控制氯化铵系数(NH4Cl加入质量与料液中V2O5的质量比)和温度.根据下图判断最佳控制氯化铵系数和温度为 、 .
(4)用硫酸酸化的H2C2O4溶液滴定(VO2)2SO4溶液,以测定反应②后溶液中含钒量,完成反应的离子方程式为□VO2++□H2C2O4+□_____=□VO2++□CO2↑+□H2O.
(5)全矾液流电池的电解质溶液为VOSO4溶液,电池的工作原理为:
VO2++V2++2H+  VO2++H2O+V3+
VO2++H2O+V3+
电池充电时阳极的电极反应式为__________________.
查看答案和解析>>
科目:高中化学 来源:2016届河北省高三下学期猜题理综化学试卷(解析版) 题型:选择题
分子式为C5H9O4N,只含有羧基和氨基两种官能团的同分异构体共有
A.8种 B.9种 C.10种 D.11种
查看答案和解析>>
科目:高中化学 来源:2016届江西省高三考前热身理综化学试卷(解析版) 题型:选择题
下列实验操作或装置符合实验要求的是 ( )
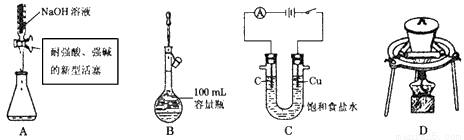
A.量取15.00 mL NaOH溶液
B.定容
C.电解制Cl2和H2
D.高温煅烧石灰石
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com