


·ÖĪö £Ø1£©ClO2·¢ÉśĘ÷ÖŠµÄ·“Ó¦ĪŖĀČĖįÄĘÓė¶žŃõ»ÆĮņŌŚÅØĮņĖį×÷ÓĆĻĀ·¢ÉśŃõ»Æ»¹Ō·“Ó¦£¬¶ųĮņ»Ē”¢ÅØĮņĖįŅ²æÉŅŌÉś³É¶žŃõ»ÆĮņ£¬ĖłŅŌæÉÓĆĮņ»Ē”¢ÅØĮņĖį“śĢęŌĮĻÖŠµÄSO2£»
£Ø2£©·“Ó¦½įŹųŗ󣬷¢ÉśĘ÷ÖŠČŌÓŠÉŁĮæClO2£¬ÓĆæÕĘųæÉŅŌ½«ĘäÅųö£¬Č·±£Ęä±»³ä·ÖĪüŹÕ£»
£Ø3£©ĪüŹÕĘ÷ÖŠĖ«ŃõĖ®ÓėClO2ŌŚ¼īŠŌĢõ¼žĻĀ·¢ÉśŃõ»Æ»¹Ō·“Ӧɜ³ÉNaClO2£¬øł¾ŻµēŗÉŹŲŗćŗĶŌŖĖŲŹŲŗćæÉŠ“³öĄė×Ó·½³ĢŹ½£¬ĪŖĮĖĢįøßClO2µÄĄūÓĆĀŹ¼°·ĄÖ¹H2O2·Ö½ā£¬·“Ó¦ĪĀ¶Č²»ÄÜøßÓŚøßÓŚ5”ę£»
£Ø4£©¢Ł¶žŃõ»ÆĮņÄܱ»ĒāŃõ»ÆÄĘČÜŅŗ»ņøßĆĢĖį¼ŲČÜŅŗĪüŹÕ£»
¢ŚDÖŠŹÕ¼Æµ½µÄĘųĢåæÉŹ¹“ųÓą½żµÄľĢõø“Č¼£¬ĖµĆ÷ÓŠŃõĘų²śÉś£¬ĖłŅŌBÖŠ·¢ÉśµÄ·“Ó¦æÉÄÜĪŖ¶žŃõ»ÆĮņÓė¹żŃõ»ÆÄĘ·“Ӧɜ³ÉŃĒĮņĖįÄĘŗĶŃõĘų£®
½ā“š ½ā£ŗ£Ø1£©ClO2·¢ÉśĘ÷ÖŠµÄ·“Ó¦ĪŖĀČĖįÄĘÓė¶žŃõ»ÆĮņŌŚÅØĮņĖį×÷ÓĆĻĀ·¢ÉśŃõ»Æ»¹Ō·“Ó¦£¬¶ųĮņ»Ē”¢ÅØĮņĖįŅ²æÉŅŌÉś³É¶žŃõ»ÆĮņ£¬·“Ó¦µÄ·½³ĢŹ½ĪŖS+2H2SO4£ØÅØ£©$\frac{\underline{\;\;”÷\;\;}}{\;}$3SO2”ü+2H2O£¬ĖłŅŌæÉÓĆĮņ»Ē”¢ÅØĮņĖį“śĢęŌĮĻÖŠµÄSO2£¬
¹Ź“š°øĪŖ£ŗS+2H2SO4£ØÅØ£©$\frac{\underline{\;\;”÷\;\;}}{\;}$3SO2”ü+2H2O£»
£Ø2£©·“Ó¦½įŹųŗ󣬷¢ÉśĘ÷ÖŠČŌÓŠÉŁĮæClO2£¬ÓĆæÕĘųæÉŅŌ½«ĘäÅųö£¬Č·±£Ęä±»³ä·ÖĪüŹÕ£¬
¹Ź“š°øĪŖ£ŗĒżøĻ³öClO2£¬Č·±£Ęä±»³ä·ÖĪüŹÕ£»
£Ø3£©ĪüŹÕĘ÷ÖŠĖ«ŃõĖ®ÓėClO2ŌŚ¼īŠŌĢõ¼žĻĀ·¢ÉśŃõ»Æ»¹Ō·“Ӧɜ³ÉNaClO2£¬·“Ó¦µÄĄė×Ó·½³ĢŹ½ĪŖ2ClO2+2OH-+H2O2=2ClO2-+O2+2H2O£¬ĪŖĮĖĢįøßClO2µÄĄūÓĆĀŹ¼°·ĄÖ¹H2O2·Ö½ā£¬·“Ó¦ĪĀ¶Č²»ÄÜøßÓŚøßÓŚ5”ę£¬
¹Ź“š°øĪŖ£ŗ2ClO2+2OH-+H2O2=2ClO2-+O2+2H2O£»ĢįøßClO2µÄĄūÓĆĀŹ¼°·ĄÖ¹H2O2·Ö½ā£»
£Ø4£©¢Ł¶žŃõ»ÆĮņÄܱ»ĒāŃõ»ÆÄĘČÜŅŗ»ņøßĆĢĖį¼ŲČÜŅŗĪüŹÕ£¬ĖłŅŌCÖŠŹ¢·ÅµÄŹŌ¼ĮĪŖNaOHČÜŅŗ£Ø»ņKMnO4ČÜŅŗ£©£¬
¹Ź“š°øĪŖ£ŗNaOHČÜŅŗ£Ø»ņKMnO4ČÜŅŗ£©£»
¢ŚDÖŠŹÕ¼Æµ½µÄĘųĢåæÉŹ¹“ųÓą½żµÄľĢõø“Č¼£¬ĖµĆ÷ÓŠŃõĘų²śÉś£¬ĖłŅŌBÖŠ·¢ÉśµÄ·“Ó¦æÉÄÜĪŖ¶žŃõ»ÆĮņÓė¹żŃõ»ÆÄĘ·“Ӧɜ³ÉŃĒĮņĖįÄĘŗĶŃõĘų£¬·“Ó¦µÄ·½³ĢŹ½ĪŖ2Na2O2+2SO2=2Na2SO3+O2£¬
¹Ź“š°øĪŖ£ŗ2Na2O2+2SO2=2Na2SO3+O2£®
µćĘĄ ±¾Ģāæ¼²éĪļÖŹµÄÖʱøŹµŃéµÄ¹¤ŅµÉč¼Ę£¬ĢāÄæÄѶČÖŠµČ£¬±¾Ģā×¢Ņā°ŃĪÕĪļÖŹµÄŠŌÖŹ£¬“ÓÖŹĮæŹŲŗćµÄ½Ē¶ČŅŌ¼°Ńõ»Æ»¹Ō·“Ó¦µÄĢŲµćÅŠ¶ĻÉś³ÉĪļ£¬ĪŖ½ā“šøĆĢāµÄ¹Ų¼ü£¬Ņ²ŹĒŅדķµć£®


 ĢģĢģĻņÉĻŅ»±¾ŗĆ¾ķĻµĮŠ“š°ø
ĢģĢģĻņÉĻŅ»±¾ŗĆ¾ķĻµĮŠ“š°ø Š”ѧɜ10·ÖÖÓÓ¦ÓĆĢāĻµĮŠ“š°ø
Š”ѧɜ10·ÖÖÓÓ¦ÓĆĢāĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| Ń”Ļī | ²Ł×÷¼°ĻÖĻó | ČÜŅŗ |
| A | ĶØČėCO2£¬ČÜŅŗ±ä»ė×Ē | ±„ŗĶNa2CO3ČÜŅŗ |
| B | ĶØČėCO2£¬ČÜŅŗ±ä»ė×Ē£¬¼ĢŠųĶØCO2ÖĮ¹żĮ棬»ė×ĒĻūŹ§ | Na2SiO3ČÜŅŗ |
| C | ĶØČėCO2£¬ČÜŅŗ±ä»ė×Ē£¬ŌŁ¼ÓČėĘ·ŗģČÜŅŗ£¬ŗģÉ«ĶŹČ„ | Ca£ØClO£©2ČÜŅŗ |
| D | ĶØČėCO2£¬ČÜŅŗ±ä»ė×Ē£¬¼ĢŠųĶØCO2ÖĮ¹żĮ棬»ė×ĒĻūŹ§£¬ŌŁ¼ÓČė×ćĮæNaOHČÜŅŗ£¬ÓÖ±ä»ė×Ē | ³ĪĒåŹÆ»ŅĖ® |
| A£® | A | B£® | B | C£® | C | D£® | D |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
| ĪĀ¶Č ŹŌ¼Į | T1/”ę | T2/”ę | T2/”ę |
| Ha2CO2 | 23.3 | 20.0 | 23.7 |
| HaCO2 | 18.5 | 20.0 | 20.8 |
| ĪĀ¶Č Čܽā¶Č | 10”ę | 20”ę | 30”ę | 40”ę |
| Ha2CO2 | 12.5g | 21.5g | 39.7g | 40£®g |
| HaHCO2 | 8.1g | 9.6g | 11.1g | 12.7 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
| ŠņŗÅ | ¢Ł | ¢Ś | ¢Ū | ¢Ü | ¢Ż | ¢Ž |
| ŅĒĘ÷¼°×°ÖĆĶ¼ | 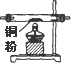 |  |  |  | 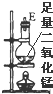 |  |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā

²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā

²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā

²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 1£ŗ3.4 | B£® | 1£ŗ1.7 | C£® | 2.6£ŗ1 | D£® | 4.6£ŗ1 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
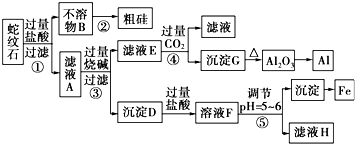
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com