某研究性学习小组做实验做实验时偶然发现,表面擦去氧化膜的镁片可与NaHCO
3溶液反应产生大量气体大量气体和白色不溶物,该小组同学通过如下实验,验证产物并探究反应原理.
实验①:用砂纸擦去镁条表面氧化膜,将其放入盛适量滴有酚酞试液的饱和碳酸氢钠溶液的烧杯中,迅速反应,产生大量气泡和白色不溶物,溶液的浅红色加深.
Ⅰ.气体的检验
实验②:将实验①中收集到的气体点燃,发现气体安静燃烧,火焰呈淡蓝色,则气体为
.
(2)该小组同学对反应中产生的白色不溶物作出如下猜测:
猜测:1:白色不溶物可能为
.
猜测2:白色不溶物可能为MgCO
3猜测3:白色不溶物可能为碱式碳酸镁[yMg(OH)
2?xMgCO
3]
请设计一个实验检验固体是否含有MgCO
3,写出实验操作,现象和结论:
.
(3)实验③:取实验①中的滤液,向其中加入少量CaCl
2稀溶液,产生白色沉淀,溶液红色变浅,说明溶液中存在CO
32-离子.
Ⅱ定量实验
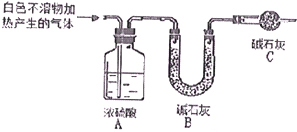
(4)为进一步确定实验Ⅰ的白色不溶物成分,进行以下的实验,装置如图所示:
称取干燥、纯净的白色不溶物7.36g,充分加热至不再产生气体为止,并使分解产生的气体全部进入装置A和B中.实验后装置A增0.72g,装置B增重2.64g,白色不溶物的化学式:
.
(5)写出镁与饱和碳酸氢钠溶液反应的化学方程式
.
Ⅲ.反应原理分析
(6)NaHCO
3溶液中存在如下电离平衡:H
2O?H
++OH
-,HCO
3-?H
++CO
32-请从平衡移动角度分析实验①产生大量气体和白色不溶物的原因:
.



 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
 某研究性学习小组做实验做实验时偶然发现,表面擦去氧化膜的镁片可与NaHCO3溶液反应产生大量气体大量气体和白色不溶物,该小组同学通过如下实验,验证产物并探究反应原理.
某研究性学习小组做实验做实验时偶然发现,表面擦去氧化膜的镁片可与NaHCO3溶液反应产生大量气体大量气体和白色不溶物,该小组同学通过如下实验,验证产物并探究反应原理.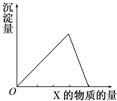 把X溶液(或气体)慢慢加入(或通入)到一定量的Y溶液中,产生的沉淀量与加入(或通入)的X物质的量的关系如图所示,符合图中曲线的是( )
把X溶液(或气体)慢慢加入(或通入)到一定量的Y溶液中,产生的沉淀量与加入(或通入)的X物质的量的关系如图所示,符合图中曲线的是( )