
| 1000ρw |
| M |
| n |
| V |
| 1.6g |
| 160g/mol |
| 4.66g |
| 233g/mol |
| 0.02mol |
| 0.1L |
| 0.04mol |
| 0.1L |
| 1000×1.20×36.5% |
| 36.5 |
| 6mol/L×0.1L |
| 12mol/L |


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
 检查装置气密性是化学实验中的重要操作之一.按要求回答下列问题:
检查装置气密性是化学实验中的重要操作之一.按要求回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Mg和Al |
| B、Mg和Zn |
| C、Fe和Zn |
| D、Cu和Fe |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、金属单质 | B、金属元素 |
| C、金属铜 | D、金属氧化物 |
查看答案和解析>>
科目:高中化学 来源: 题型:
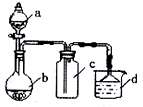 实验室某些气体的制取、收集及尾气处理装置如图所示(省略夹持和净化装置).用此装置和表中提供的物质完成相关实验,最合理的选项是( )
实验室某些气体的制取、收集及尾气处理装置如图所示(省略夹持和净化装置).用此装置和表中提供的物质完成相关实验,最合理的选项是( )| 选项 | a中物质 | b中物质 | c中收集气体 | d中物质 |
| A | 浓氨水 | CaO | NH3 | H2O |
| B | 浓硝酸 | Cu | NO2 | H2O |
| C | 浓硫酸 | Na2SO3 | SO2 | NaOH溶液 |
| D | 浓盐酸 | KClO3 | Cl2 | 澄清石灰水 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Cu2+、Na+、SO42-、Cl- |
| B、K+、H+、HCO3-、NO3- |
| C、OH-、HCO3-、Ca2+、Na+ |
| D、Ba2+、Na+、OH-、NO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、0.1mol.L-1的NaHCO3溶液中离子浓度关系:c(Na+)=2c(CO32-)+2c(HCO3-)+2c(H2CO3) | ||||
B、室温下,将物质的量浓度相等的一元酸HA和KOH等体积混合,溶液的pH=9,则:c(OH-)=c(K+)-c(A-)=
| ||||
C、将HCN和HF溶液混合,达平衡时:c(H+)=
| ||||
| D、等物质的量的CH3COOH和CH3COONa配置成混合溶液,已知其中c(CH3COO-)>c(Na+),则c(CH3COOH)<c(CH3COO-) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、铜氨溶液的制备:Cu2-+2NH3.H2O=Cu(NH3)22++2H2O |
| B、氢氧化钡溶液中滴加明矾溶液至Ba2+恰好完全沉淀:Ba2++30H-+SO42-+Al3+=BaSO4↓+Al(OH)3↓ |
C、水杨酸钠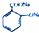 通入过量的CO2; 通入过量的CO2;  +CO2+H2O→ +CO2+H2O→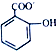 +HCO3- +HCO3- |
| D、在氯化亚铁溶液中加入足量酸性高锰酸钾溶液:5Fe2++8H++Mn04-=5Fe3++Mn2++4H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、焓变 | B、温度 | C、压强 | D、熵变 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com