
| A. | 2NO(g)+O2(g)═2NO2(g) | B. | 2C2H6(g)+7O2(g)═4CO2(g)+6H2O(g) | ||
| C. | NH4NO3(s)═NH4+(aq)+NO3-(aq) | D. | H2(g)+Cl2(g)═2HCl(l) |
分析 根据方程式中各物质的聚集状态判断反应的熵变,根据反应过程中反应物和生成物能量高低判断反应的焓变.
解答 解:A.2NO(g)+O2(g)═2NO2(g)反应中气体的物质的量减小,所以熵减小,即△S<0,故A错误;
B.2C2H6(g)+7O2(g)═4CO2(g)+6H2O(g)反应中气体的物质的量减小,所以熵减小,即△S<0,故B错误;
C.NH4NO3(s)═NH4+(aq)+NO3-(aq)该反应为吸热过程,即△H>0,故C错误;
D.H2(g)+Cl2(g)═2HCl(l)该反应为放热反应,即△H<0,反应后气体的物质的量减小,则△S>0,故D正确.
故选D.
点评 本题考查了反应的焓变和熵变,题目难度不大,根据物质的状态来判断熵变的大小,注意把握常见的吸热反应和放热反应.


 挑战100单元检测试卷系列答案
挑战100单元检测试卷系列答案 名题金卷系列答案
名题金卷系列答案科目:高中化学 来源: 题型:解答题
| 时间(s) | 0 | 10 | 20 | 25 | 30 |
| 条件A[n(NO2)](mol) | 0.20 | 0.14 | 0.13 | 0.13 | 0.13 |
| 条件B[n(NO2)](mol) | 0.20 | 0.10 | 0.10 | 0.10 | 0.10 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
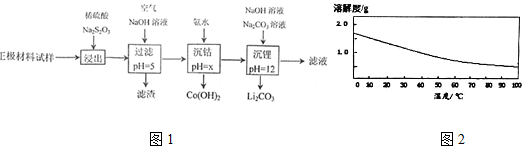
| 氢氧化物 | Al(OH)3 | Fe(OH)3 | Fe(OH)3 |
| 开始沉淀的pH | 3.1 | 7.1 | 2.2 |
| 完全沉淀的pH | 4.7 | 9.7 | 3.7 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com