
(12分) 天然气(主要成分甲烷)是一种清洁、高效的能源,现在许多城市家庭用于厨房使用的燃料已经由煤气(主要成分是H2和CO按体积比1︰1混合的气体混合物)换成了天然气;此外天然气也是很好的燃料电池的燃料,甲烷在燃料电池中的能量转换率可达到85%—90%。请回答下列问题:
⑴已知H2、CO和CH4的燃烧热分别是286kJ/mol、283 kJ/mol和890 kJ/mol,则反应2CH4(g)+3O2(g)=CO(g)+H2(g)+CO2(g)+3H2O(l)的反应热 △H= 。
⑵以甲烷、空气为反应物,KOH溶液作电解质溶液构成燃料电池,则负极反应式为: 。随着反应的不断进行溶液的pH (填“增大”“减小”或“不变”)。
⑶如果以该燃料电池为电源、石墨作两极电解饱和食盐水,则该电解过程中阳极反应式为: ;如果电解一段时间后NaCl溶液的体积为1L,溶液的pH为12,则理论上消耗甲烷在标准状况下的体积为: mL。
⑷将⑶中电解结束后的溶液取出,向其中加入含有Mg2+和Fe2+的溶液甲,Mg(OH)2和Fe(OH)2同时生成,已知Mg(OH)2和Fe(OH)2在该温度下的溶度积常数分别是2×10—11和8×10—16,则甲溶液中Mg2+和Fe2+的浓度比为: 。
 全能测控期末小状元系列答案
全能测控期末小状元系列答案科目:高中化学 来源: 题型:阅读理解
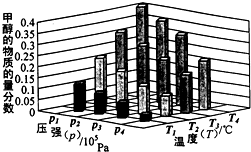 能源是制约国家发展进程的因素之一.甲醇、二甲醚等被称为2 1世纪的绿色能源,工业上利用天然气为主要原料与二氧化碳、水蒸气在一定条件下制备合成气(CO、H2),再制成甲醇、二甲醚.
能源是制约国家发展进程的因素之一.甲醇、二甲醚等被称为2 1世纪的绿色能源,工业上利用天然气为主要原料与二氧化碳、水蒸气在一定条件下制备合成气(CO、H2),再制成甲醇、二甲醚.查看答案和解析>>
科目:高中化学 来源:2011-2012学年四川省成都市六校协作体高二下学期期中联考化学试卷(带解析) 题型:填空题
(12分)合成气的主要成分是一氧化碳和氢气,可用于合成二甲醚等清洁燃料。从天然气获得合成气过程中可能发生的反应有:
①CH4(g)+H2O(g) CO(g)+3H2(g) ⊿H1="+206.1" kJ/mol
CO(g)+3H2(g) ⊿H1="+206.1" kJ/mol
②CH4(g)+CO2(g) 2CO(g)+2H2(g) ⊿H2="+247.3" kJ/mol
2CO(g)+2H2(g) ⊿H2="+247.3" kJ/mol
③CO(g)+H2O(g) CO2(g)+ H2(g) ⊿H3
CO2(g)+ H2(g) ⊿H3
请回答下列问题:
(1)在一密闭容器中进行反应①,测得 的物质的量浓度随反应时间的变化如图1所示。10min时,改变的外界条件可能是 。
的物质的量浓度随反应时间的变化如图1所示。10min时,改变的外界条件可能是 。
(2)如图2所示,在甲、乙两容器中分别充入等物质的量的 和
和 ,使甲、乙两容器初始容积相等。在相同温度下发生反应②,并维持反应过程中温度不变。已知甲容器中
,使甲、乙两容器初始容积相等。在相同温度下发生反应②,并维持反应过程中温度不变。已知甲容器中 的转化率随时间变化的图像如图3所示,请在图3中画出乙容器中
的转化率随时间变化的图像如图3所示,请在图3中画出乙容器中 的转化率随时间变化的图像。
的转化率随时间变化的图像。
(3)反应③中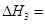 。800℃时,反应③的化学平衡常数K=1.0,某时刻测得该温度下的密闭容器中各物质的物质的量见下表:
。800℃时,反应③的化学平衡常数K=1.0,某时刻测得该温度下的密闭容器中各物质的物质的量见下表:
此时反应③中正、逆反应速率的关系式是 (填代号)。
a. (正)
(正) (逆) b.
(逆) b. (正)<
(正)< (逆) c.
(逆) c. (正)=
(正)= (逆) d.无法判断
(逆) d.无法判断
(4)800K时下列起始体积相同的密闭容器中充入2mol SO2、1mol O2,其反应是2SO2(g)+O2(g)  2SO3(g);△H=-96.56 kJ?mol-1,甲容器在反应过程中保持压强不变,乙容器保持体积不变,丙容器维持绝热,三容器各自建立化学平衡。
2SO3(g);△H=-96.56 kJ?mol-1,甲容器在反应过程中保持压强不变,乙容器保持体积不变,丙容器维持绝热,三容器各自建立化学平衡。
【1】达到平衡时,平衡常数K (甲) K (乙) K(丙)(填“>”、“<”或“=”)。
【2】达到平衡时SO2的浓度C(SO2)(甲) C(SO2) (乙) C(SO2) (丙)(填“>”、“<”或“=”)。
查看答案和解析>>
科目:高中化学 来源:2011届黑龙江省哈三中等四校高三第一次高考模拟联考(理综)化学部分 题型:填空题
(12分) 天然气(主要成分甲烷)是一种清洁、高效的能源,现在许多城市家庭用于厨房使用的燃料已经由煤气(主要成分是H2和CO按体积比1︰1混合的气体混合物)换成了天然气;此外天然气也是很好的燃料电池的燃料,甲烷在燃料电池中的能量转换率可达到85%—90%。请回答下列问题:
⑴已知H2、CO和CH4的燃烧热分别是286kJ/mol、283 kJ/mol和890 kJ/mol,则反应2CH4(g)+3O2(g)=CO(g)+H2(g)+CO2(g)+3H2O(l)的反应热△H= 。
⑵以甲烷、空气为反应物,KOH溶液作电解质溶液构成燃料电池,则负极反应式为: 。随着反应的不断进行溶液的pH (填“增大”“减小”或“不变”)。
⑶如果以该燃料电池为电源、石墨作两极电解饱和食盐水,则该电解过程中阳极反应式为: ;如果电解一段时间后NaCl溶液的体积为1L,溶液的pH为12,则理论上消耗甲烷在标准状况下的体积为: mL。
⑷将⑶中电解结束后的溶液取出,向其中加入含有Mg2+和Fe2+的溶液甲,Mg(OH)2和Fe(OH)2同时生成,已知Mg(OH)2和Fe(OH)2在该温度下的溶度积常数分别是2×10—11和8×10—16,则甲溶液中Mg2+和Fe2+的浓度比为: 。
查看答案和解析>>
科目:高中化学 来源:2010-2011学年黑龙江省等四校高三第一次高考模拟联考(理综)化学部分 题型:填空题
(12分) 天然气(主要成分甲烷)是一种清洁、高效的能源,现在许多城市家庭用于厨房使用的燃料已经由煤气(主要成分是H2和CO按体积比1︰1混合的气体混合物)换成了天然气;此外天然气也是很好的燃料电池的燃料,甲烷在燃料电池中的能量转换率可达到85%—90%。请回答下列问题:
⑴已知H2、CO和CH4的燃烧热分别是286kJ/mol、283 kJ/mol和890 kJ/mol,则反应2CH4(g)+3O2(g)=CO(g)+H2(g)+CO2(g)+3H2O(l)的反应热 △H= 。
⑵以甲烷、空气为反应物,KOH溶液作电解质溶液构成燃料电池,则负极反应式为: 。随着反应的不断进行溶液的pH (填“增大”“减小”或“不变”)。
⑶如果以该燃料电池为电源、石墨作两极电解饱和食盐水,则该电解过程中阳极反应式为: ;如果电解一段时间后NaCl溶液的体积为1L,溶液的pH为12,则理论上消耗甲烷在标准状况下的体积为: mL。
⑷将⑶中电解结束后的溶液取出,向其中加入含有Mg2+和Fe2+的溶液甲,Mg(OH)2和Fe(OH)2同时生成,已知Mg(OH)2和Fe(OH)2在该温度下的溶度积常数分别是2×10—11和8×10—16,则甲溶液中Mg2+和Fe2+的浓度比为: 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com