
【题目】浓硫酸分别与三种钠盐反应,现象如图。下列分析正确的是( )
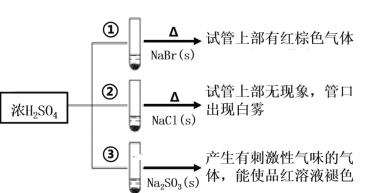
A.②中试管口白雾是HCl遇水蒸气所致,说明酸性:H2SO4>HCl
B.①和③相比可说明氧化性:Br2>SO2
C.对比①和②可以说明还原性:Br->Cl-
D.③中浓H2SO4被还原成SO2
【答案】C
【解析】
A、利用浓硫酸高沸点,HCl易挥发,反应②利用高沸点酸制取低沸点酸,不能得出酸性强弱,A选项错误;
B、反应①出现红棕色气体,说明产生Br2(g),Br-被氧化;反应③产生的气体为SO2,反应③发生Na2SO3+H2SO4=Na2SO4+SO2↑+H2O,不属于氧化还原反应,不能说明Br2的氧化性强于SO2,B选项错误;
C、反应①出现红棕色气体,说明产生Br2(g),Br-被氧化,反应②管口出现白雾,白雾是HCl的小液滴,Cl-没有被氧化,说明Br-的还原性强于Cl-,C选项正确;
D、反应③的方程式为Na2SO3+H2SO4=Na2SO4+SO2↑+H2O,不属于氧化还原反应,D选项错误;
答案选C。


 超能学典应用题题卡系列答案
超能学典应用题题卡系列答案科目:高中化学 来源: 题型:
【题目】下列各组物质
①O2和O3 ②H2、D2、T2 ③12C和14C ④CH3CH2CH2CH3和(CH3)2CHCH3 ⑤乙烷和丁烷 ⑥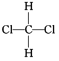 和
和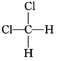 ⑦
⑦![]() 和
和![]() ⑧氯气和氯水 ⑨红磷和白磷
⑧氯气和氯水 ⑨红磷和白磷
互为同位素的是___(填序号,下同),互为同素异形体的是___,互为同系物的是__,互为同分异构体的是__,属于同一物质的是__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)在①CO2,②NaCl,③Na,④Si,⑤CS2,⑥金刚石,⑦(NH4)2SO4,⑧乙醇中,由极性键形成的非极性分子有_______(填序号,以下同),含有金属离子的物质是__,分子间可形成氢键的物质是________,属于离子晶体的是__,属于原子晶体的是__,①~⑤五种物质的熔点由高到低的顺序是__。
(2)A,B,C,D为四种晶体,性质如下:
A.固态时能导电,能溶于盐酸
B.能溶于CS2,不溶于水
C.固态时不导电,液态时能导电,可溶于水
D.固态、液态时均不导电,熔点为3500 ℃
试推断它们的晶体类型:A.__;B.__;C.__;D.__。
(3)下图中A~D是中学化学教科书上常见的几种晶体结构模型,请填写相应物质的名称:A.__;B.__;C.__D.____。
.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】丁苯酞( )是一种治疗脑血管疾病的药物,它的一种合成路线如图:
)是一种治疗脑血管疾病的药物,它的一种合成路线如图:

已知:
(1)Y的名称是_____。
(2)H的结构简式为___。
(3)X→Y的反应类型是_____。H→丁苯酚的“一定条件”指_____。
(4)写出W→X的化学方程式:_____。
(5)W的二溴代物有___种,其中一种在核磁共振氢谱上有3组峰的结构为___(填结构简式)。
(6)以某烯烃为原料合成(CH3)3CMgBr,参照上述流程,设计合成路线。___
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是一种航天器能量储存系统原理示意图。下列说法正确的是
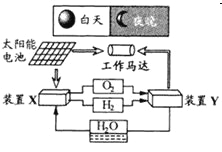
A. 该系统中只存在3种形式的能量转化
B. 装置Y中负极的电极反应式为:![]()
C. 装置X能实现燃料电池的燃料和氧化剂再生
D. 装置X、Y形成的子系统能实现物质的零排放,并能实现化学能与电能间的完全转化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某校化学研究性学习小组查阅资料了解到以下内容:
乙二酸(HOOC﹣COOH,可简写为H2C2O4)俗称草酸,易溶于水,属于二元中强酸(为弱电解质),且酸性强于碳酸,其熔点为101.5℃,在157℃升华.为探究草酸的部分化学性质,进行了如下实验:
(1)向盛有1mL饱和NaHCO3溶液的试管中加入足量乙二酸溶液,观察到有无色气泡产生.该反应的离子方程式为________;
(2)向盛有乙二酸饱和溶液的试管中滴入几滴硫酸酸化的KMnO4溶液,振荡,发现其溶液的紫红色褪去;①说明乙二酸具有______(填“氧化性”、“还原性”或“酸性”);②请配平该反应的离子方程式:_____MnO4-+____H2C2O4+___H+=___Mn2++____CO2↑+_____H2O
(3)将一定量的乙二酸放于试管中,按如图所示装置进行实验(夹持装置未标出):

实验发现:装置C、G中澄清石灰水变浑浊,B中CuSO4粉末变蓝,F中CuO粉末变红。据此回答:
①上述装置中,D的作用是_________,
②乙二酸分解的化学方程式为 ________;
(4)该小组同学将2.52g草酸晶体(H2C2O42H2O)加入到100mL 0.2mol/L的NaOH溶液中充分反应,测得反应后溶液呈酸性,其原因是_______(用文字简单表述),该溶液中各离子的浓度由大到小的顺序为:_______(用离子符号表示).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有A、B、C、D、E五种元素,它们的质子数依次增多。
①A的核电荷数大于2,可形成氢化物H2A,该氢化物在常温下是液体;
②A和B两元素可形成B2A3化合物,该化合物既能溶于强酸,又能溶于强碱;
③C+离子比B3+离子多8个电子;
④C与D元素可以形成化合物CD;
⑤CD的溶液中通入氯气后加淀粉溶液显蓝色;
⑥E、C同主族,且E比C多两个电子层,E单质可与冷水反应生成氢气.
试回答:
(1)A在元素周期表中的位置___,B的离子结构示意图___,化合物NH4D(含D-的铵盐)的电子式___。
(2)C的某种简单阳离子,其原子核中含22个中子,其化学符号为___;元素D最高价氧化物的水化物化学式为___。
(3)B、C、E三种元素的金属性按照由强到弱的顺序排列应为:___(用元素符号表示)。
(4)写出单质B和氢氧化钠溶液反应的离子方程式:___。
(5)写出E与冷水反应的离子方程式:___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下,将浓度都是0.1mol·L-1的X2、Y2两种气体充入至密闭容器中,使之发生反应生成气体Z,达到平衡时c(X2)=0.04mol·L-1、c(Y2)=0.08mol·L-1、c(Z)=0.04mol·L-1,则该反应的反应式是
A. X2+2Y2![]() XY2 B. 3X2+Y2
XY2 B. 3X2+Y2![]() 2X3Y
2X3Y
C. 2X2+Y2![]() 2X2Y D. X2+3Y2
2X2Y D. X2+3Y2![]() 2XY3
2XY3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在两份相同的Ba(OH)2溶液中,分别滴入物质的量浓度相等的H2SO4、NaHSO4溶液,其导电能力随滴入溶液体积变化的曲线如右图所示。下列分析不正确的是( )

A. ①代表滴加H2SO4溶液的变化曲线
B. b点,溶液中大量存在的离子是Na+、OH–
C. c点,两溶液中含有相同量的OH–
D. a、d两点对应的溶液均显中性
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com