
| A. | ①②③④⑤⑥ | B. | ②③⑤ | C. | ①②④⑤ | D. | ①③⑤ |
分析 ①新制氯水中含有大量氯气和次氯酸,久置氯水相当于盐酸溶液;
②氯气的性质活泼,它与氢气混合后干燥条件下发生爆炸;
③氯气有毒,不能直接排空,要有尾气处理装置;
④氯气、HCl都可以和硝酸银反应生成白色沉淀;
⑤HCl极易溶于水、饱和氯化钠溶液抑制氯气溶解;
⑥氯气没有漂白性,次氯酸有漂白性.
解答 解:①新制氯水中含有大量氯气和次氯酸,久置氯水相当于盐酸溶液,氯水和次氯酸有强氧化性、盐酸具有弱氧化性,所以新制氯水氧化性大于久置氯水,故正确;
②氯气的性质活泼,它与氢气混合后干燥条件下发生爆炸,常温下不反应,故错误;
③氯气有毒不能直接排空,氯气和水反应生成酸,所以氯气能和碱反应生成盐,实验室用NaOH溶液吸收氯气尾气,故正确;
④氯气、HCl都可以和硝酸银反应生成白色沉淀,所以不能用硝酸银溶液检验,故错误;
⑤HCl极易溶于水,饱和食盐水抑制氯气溶解,所以可以用饱和食盐水除去氯气中的HCl,故正确;
⑥氯气没有漂白性,次氯酸有漂白性,干燥的氯气能使湿润的有色布条褪色,实际上是氯气和水反应生成的HClO体现的漂白性,故错误;
故选D.
点评 本题考查氯气、氯水的性质,知道氯水中成分及其性质是解本题关键,知道氯气的收集方法、次氯酸的漂白性,注意氯气没有漂白性,为易错点.


科目:高中化学 来源: 题型:选择题
| A. | 在水溶液中能导电的化合物都是电解质 | |
| B. | 在熔融状态下不导电的化合物都是非电解质 | |
| C. | 氨水为混合物,不属于电解质 | |
| D. | 硫酸溶于水能导电,所以浓硫酸为电解质 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1.12 | B. | 2.24 | C. | 2.8 | D. | 4.48 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
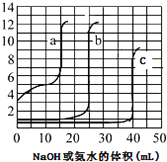 取未知浓度的硫酸、盐酸和醋酸各25.00mL,分別用0.10mol•L-1的NaOH溶液或0.10mol•L-1 的稀氨水滴定得如图.下列说法正确的是( )
取未知浓度的硫酸、盐酸和醋酸各25.00mL,分別用0.10mol•L-1的NaOH溶液或0.10mol•L-1 的稀氨水滴定得如图.下列说法正确的是( )| A. | 由图可知曲线c为NaOH滴定硫酸 | |
| B. | 由图可知硫酸的物质的量浓度大于盐酸的物质的量浓度 | |
| C. | 曲线b、c的滴定实验可用酚酞做指示剂 | |
| D. | 由图可知滴定前醋酸电离度约为1.67% |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
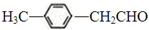 转化为对甲基苯乙炔
转化为对甲基苯乙炔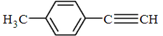 的合成路线流程图如下:
的合成路线流程图如下: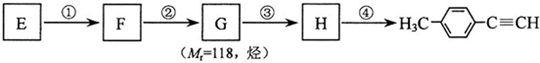
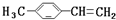 ,③的反应类型为加成反应.
,③的反应类型为加成反应. .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向烧碱溶液中通入少量的二氧化碳 2OH-+CO2=CO32-+H2O | |
| B. | 向氯化铝溶液中滴加过量浓氨水 Al3++3OH-═Al(OH)3↓ | |
| C. | 向水玻璃中通入少量二氧化碳 SiO32-+CO2+H2O=H2SiO3↓+CO32- | |
| D. | 铝与氢氧化钠溶液反应 2Al+2OH-+6H2O═2AlO2-+3H2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | C5H12有2种同分异构体 | |
| B. | C8H10中只有三种属于芳香烃的同分异构体 | |
| C. | CH3CH2CH2CH3光照下与氯气反应,只生成一种一氯代烃 | |
| D. | 甲苯苯环上的一个氢原子被含3个碳原子的烷基取代,所得产物有6种 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
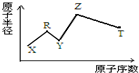 现有短周期主族元素X、Y、Z、R、T.R原子最外层电子数是电子层数的2倍;Y与Z能形成Z2Y、Z2Y2型离子化合物,Z与T形成的Z2T 化合物能破坏水的电离平衡.六种元素的原子半径与原子序数的关系如图所示.下列推断正确的是( )
现有短周期主族元素X、Y、Z、R、T.R原子最外层电子数是电子层数的2倍;Y与Z能形成Z2Y、Z2Y2型离子化合物,Z与T形成的Z2T 化合物能破坏水的电离平衡.六种元素的原子半径与原子序数的关系如图所示.下列推断正确的是( )| A. | 原子半径和离子半径均满足:Y<Z | |
| B. | 氢化物的沸点排序:Y>T>R | |
| C. | 最高价氧化物对应的水化物的酸性:T<R | |
| D. | 由X、R、Y、Z四种元素组成的化合物水溶液一定显碱性 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com