
| 滴定次数实验数据 | 1 | 2 | 3 |
| V(样品)/mL | 20.00 | 20.00 | 20.00 |
| V(KMnO4)/mL(初读数) | 0.00 | 0.20 | 0.00 |
| V(KMnO4)/mL(终读数) | 15.85 | 15.22 | 14.98 |
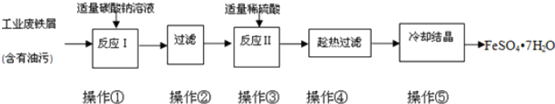
分析 (1)CO32-水解生成OH-,溶液显碱性,酯在碱性条件下完全水解;
(2)由于硫酸亚铁的溶解度随温度的升高二增大;
(3)①转移液体需要引流;
②硝酸有强氧化性,盐酸有还原性;高锰酸钾有强氧化性,应放在酸式滴定管中;滴定终点时,颜色变成紫红色,并且半分钟内不褪色;
③配平反应的离子方程式:5Fe2++MnO4-+8H+═5Fe3++Mn2++4H2O,根据方程式进行计算,滴定中由于第一组数据误差较大,应舍去,以此计算.
解答 解:(1)CO32-水解生成OH-,溶液显碱性,酯在碱性条件下完全水解,所以可用纯碱溶液除油污,
故答案为:除去废铁屑表面的油污;
(2)由于硫酸亚铁的溶解度随温度的升高二增大,因此用冰水洗涤的另一个目的是减少洗涤过程中FeSO4•7H2O的损耗,
故答案为:降低FeSO4在水中的溶解度,减少FeSO4•7H2O的损耗;
(3)①转移液体需要引流,玻璃棒底部要在容量瓶的刻度线以下且玻璃棒不能碰到容量瓶口,
故答案为:用玻璃棒引流,玻璃棒底部要在容量瓶的刻度线以下且玻璃棒不能碰到容量瓶口;
②硝酸有强氧化性,盐酸有还原性,能被高能酸钾氧化为氯气,只能用稀硫酸,故选c;
高锰酸钾有强氧化性,能氧化橡皮管,应放在酸式滴定管中;
滴定终点时,颜色变成紫红色,并且半分钟内不褪色,否则不可以判断达到终点;
故答案为:c;酸式;滴入最后一滴KMnO4溶液,恰好变为紫红色,且半分钟内不退色;
③配平反应的离子方程式:5Fe2++MnO4-+8H+═5Fe3++Mn2++4H2O,滴定中由于第一组数据误差较大,应舍去,
反应需要的高锰酸钾的物质的量为$\frac{15.02+14.98}{2}$×10-3L×1.2×10-2mol/L=18×10-5mol
则:5Fe2++MnO4-+8H+═5Fe3++Mn2++4H2O
5mol 1mol
n 18×10-5mol
n=18×10-5mol×5=90×10-5mol,
则1.500g硫酸亚铁补血剂药片含铁的质量为90×10-5mol×5×56g/mol=0.252g,所以该补血剂中铁元素的含量为$\frac{0.252g}{1.5g}$×100%=16.8%,
故答案为:16.8%.
点评 本题考查了铁及其化合物性质的分析判断和反应产物的计算判断,元素守恒、元素化合价是解题关键,题目难度中等.


 第1卷单元月考期中期末系列答案
第1卷单元月考期中期末系列答案科目:高中化学 来源: 题型:选择题
| A. | 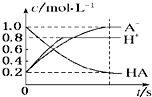 | B. | 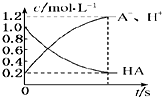 | ||
| C. |  | D. |  |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①③⑤⑧⑨ | B. | ②④⑤⑧⑨ | C. | ①②③⑤⑦ | D. | ③⑤⑥⑦⑧⑨ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 发酵粉--Na2CO3 | B. | 化肥碳铵--(NH4)2CO3 | ||
| C. | 漂白粉的有效成分Ca(ClO)2 | D. | 月饼中的抗氧化剂--CaO |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | (1)、(4) | B. | 只有(3) | C. | 只有(2) | D. | (1)(2)(3)(4) |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
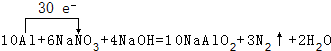 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在熔融态能导电的物质一定是电解质 | |
| B. | 能溶于水且水溶液能导电的化合物是电解质 | |
| C. | 易溶性强电解质的水溶液中只有离子没有分子 | |
| D. | 饱和水溶液导电能力弱的电解质未必是弱电解质 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 离子 | Cu2+ | H+ | Cl- | SO42- |
| c/mol•L-1 | 0.5 | 2 | 2 | 0.5 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| T/℃ | 700 | 800 | 830 | 1000 | 1200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com