含钡化合物在实验室和工业生产中都有广泛的用途.
(1)过氧化钡(BaO
2)是一种常用的氧化剂,还可用于生产钡盐.工业上制取过氧化钡的方法之一是2BaO+O
22BaO
2.现有16.0吨的氧化钡在足量的氧气中加热反应后,固体的质量变为17.6吨.那么实际参加反应的氧化钡的质量为
吨.
(2)某同学查得Ba(OH)
2?8H
2O晶体在20℃时的溶解度为3.9g/100g水,则20℃时,Ba(OH)
2饱和溶液的质量分数为
(答案保留2位小数).
(3)取不同质量由Ba(OH)
2?nH
2O和BaCO
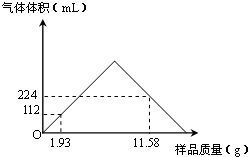
3组成的样品,加水溶解后加入80mL 1.0mol/L的盐酸,并不断地搅拌,所得CO
2气体的体积(已换算为标准状况)与加入样品的质量关系通过描点得到下图(在此过程中不考虑Ba(HCO
3)
2的生成和CO
2的溶解).请计算:
①在11.58g样品中BaCO
3的质量为多少g?
②化学式Ba(OH)
2?nH
2O中n的值为多少?
(4)含钡的矿物大多是重晶石(主要成分是BaSO
4),工业上常用天然气在850~900℃的条件下还原BaSO
4生产BaS.发生反应的化学方程式有:
BaSO
4+CH
4(少量)→BaS+CO
2+2H
2O
3BaSO
4+4CH
4(足量)→3BaS+4CO+8H
2O
①若反应后混合气体中CO
2的体积分数为
,求该反应条件下混合气体的平均式量?
(假设每步反应都完全.答案保留2位小数)
②实际工业生产中,天然气很难反应完全.现有2.0×10
6 mol的CH
4,若CH
4的利用率为95%,且反应结束后高温气体中CO的体积分数为0.02,求能生产多少吨BaS?(答案保留2位小数)



 含钡化合物在实验室和工业生产中都有广泛的用途.
含钡化合物在实验室和工业生产中都有广泛的用途.