
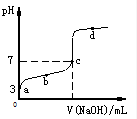
 ��֪ij�¶�ʱCH3COOH�ĵ���ƽ�ⳣ��ΪK�����¶�����20mL0.1mol/LCH3COOH��Һ����μ���0.1mol/L NaOH��Һ����pH�仯������ͼ��ʾ�������¶ȱ仯��������˵������ȷ���ǣ�������
��֪ij�¶�ʱCH3COOH�ĵ���ƽ�ⳣ��ΪK�����¶�����20mL0.1mol/LCH3COOH��Һ����μ���0.1mol/L NaOH��Һ����pH�仯������ͼ��ʾ�������¶ȱ仯��������˵������ȷ���ǣ�������| A�� | a ���ʾ����Һ��c��CH3COO-����10-3mol/L | |
| B�� | b ���ʾ����Һ��c��Na+����c��CH3COO-�� | |
| C�� | c ���ʾCH3COOH��NaOHǡ�÷�Ӧ��ȫ | |
| D�� | b��d ���ʾ����Һ��$\frac{c��C{H}_{3}CO{O}^{-}��•c��{H}^{+}��}{c��C{H}_{3}COOH��}$������K |
���� A��a��pH=3����CH3COOH�TCH3COO-+H+������
B��b����Һ�����ԣ��ɵ���غ������
C��c����Һ��pH=7��
D��b��d ���¶Ȳ��䣬��K���䣮
��� �⣺A��a��pH=3����CH3COOH?CH3COO-+H+��֪��c��H+��=c��CH3COO-��=10-3mol/L����A����
B��b����Һ�����ԣ�c��H+����c��OH-�����ɵ���غ��֪��c��Na+����c��CH3COO-������B����
C��c����Һ��pH=7����CH3COOH��NaOHǡ�÷�Ӧ��ȫ���ɴ����ƣ���Һ��pH��7��Ӧ����ʣ�࣬��C����
D��$\frac{c��C{H}_{3}CO{O}^{-}��•c��{H}^{+}��}{c��C{H}_{3}COOH��}$=K��b��d ���¶Ȳ��䣬��K���䣬����b��d ���ʾ����Һ��$\frac{c��C{H}_{3}CO{O}^{-}��•c��{H}^{+}��}{c��C{H}_{3}COOH��}$������K����D��ȷ��
��ѡD��
���� ���⿼���������Һ�Ķ����жϣ���ȷͼ���и����pH����Һ�е����ʼ��ɽ��ע�����غ㼰����ƽ�ⳣ��ֻ���¶��йأ���Ŀ�ѶȲ���


 �Ͻ�ƽ��У����ϵ�д�
�Ͻ�ƽ��У����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
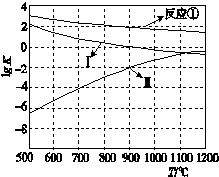 ��CaSO4����O2��ȼ��CO��Ӧ���ȿ����ȼ��Ч�ʣ����ܵõ��ߴ�CO2����һ�ָ�Ч����ࡢ���õ�����ȼ�ռ�������Ӧ��Ϊ����Ӧ����Ӧ�ں͢�Ϊ����Ӧ��
��CaSO4����O2��ȼ��CO��Ӧ���ȿ����ȼ��Ч�ʣ����ܵõ��ߴ�CO2����һ�ָ�Ч����ࡢ���õ�����ȼ�ռ�������Ӧ��Ϊ����Ӧ����Ӧ�ں͢�Ϊ����Ӧ���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���� | B�� | ������ | C�� | ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����128g Sʱ����Ӧת�Ƶĵ��������ʵ���Ϊ164mol | |
| B�� | ����12gCʱ����Ӧת��4mol���� | |
| C�� | �������ͱ���ԭ����ԭ��֮��Ϊ3��1 | |
| D�� | KNO3������������Ӧ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
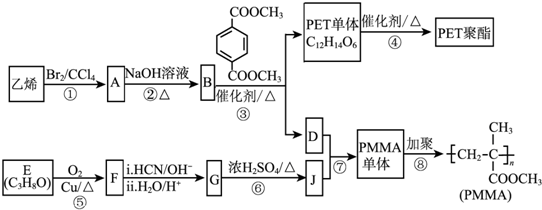
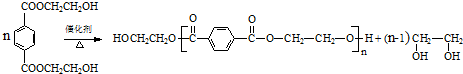
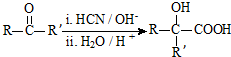 ��R��R�����������
��R��R�����������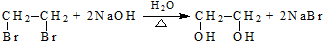 ��
��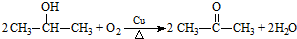 ��
��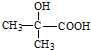 ��
��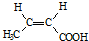 ��
�� ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ʳ�� | B�� | ζ�� | C�� | �������� | D�� | ʳ�� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com