
| A. | 3:1 | B. | 3:2 | C. | 2:1 | D. | 1:2 |
分析 假设全部为NO2,通入水中,发生反应:3NO2+H2O=2HNO3+NO,剩余体积为原体积的$\frac{1}{3}$,而实际混合气体反应量筒内的气体体积减小为原来的一半,说明剩余气体为氧气,发生反应:4NO2+O2+2H2O=4HNO3,设混合气体中含有xmolO2,ymolNO2,根据方程式表示出参加反应的氧气,再根据体积之比列方程计算.
解答 解:假设全部为NO2,通入水中,发生反应:3NO2+H2O=2HNO3+NO,剩余体积为原体积的$\frac{1}{3}$,而实际混合气体反应量筒内的气体体积减小为原来的一半,说明剩余气体为氧气,
设混合气体中含有xmolO2,ymolNO2,则:
4 NO2+O2+2H2O=4HNO3,
ymol $\frac{1}{4}$ymol
所以(x-$\frac{1}{4}$y):(x+y)=1:2,
整理得x:y=3:2,
故选B.
点评 本题考查混合物的计算,题目难度中等,关键是利用假设法判断剩余气体为氧气,侧重考查学生分析计算能力.


 同步练习西南师范大学出版社系列答案
同步练习西南师范大学出版社系列答案 补充习题江苏系列答案
补充习题江苏系列答案 学练快车道口算心算速算天天练系列答案
学练快车道口算心算速算天天练系列答案科目:高中化学 来源: 题型:选择题
| A. | 在1 mol CaC2、KHSO4、KO2(超氧化钾)三种离子化合物中,所含阴、阳离子的总数均为3NA | |
| B. | 0.1 mol C2H2OH中所含C-H键的数目为0.6NA | |
| C. | S2和S8的混合物共6.4g,其中所含硫原子数一定为0.2NA | |
| D. | 78gNa2O2与足量水反应转移的电子数为2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 构成单质分子的微粒一定含有共价键 | |
| B. | 全部由非金属元素形成的化合物不一定只含共价键 | |
| C. | 离子化合物中不可能含有非极性键 | |
| D. | 非极性键只存在于双原子单质分子中 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | [H+]=[OH-]的溶液 | B. | pH<7的溶液 | ||
| C. | [H+]=1.0×10-7mol•L-1 的溶液 | D. | [H+]>[OH-]的溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 甲酸能与水以任意比互溶 | |
| B. | 0.1mol/L的甲酸钠溶液的pH约为9 | |
| C. | 0.1mol/L的甲酸溶液的pH约为4.8 | |
| D. | 10mL0.1mol/L的甲酸恰好能与10mL0.1mol/L的NaOH溶液完全反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 10gD2O中含有的电子数为5NA | |
| B. | 1molC3H8分子中共价键总数为10NA | |
| C. | 92gNO2和N2O4混合气体中含有原子数为3NA | |
| D. | 65gZn全部溶解在一定浓度的硝酸溶液中,有NO生成,则转移的电子数为2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
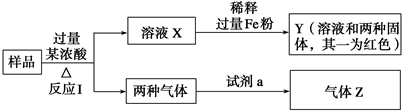
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 将白炽灯换成节能灯 | B. | 少开汽车,多骑自行车或坐公交车 | ||
| C. | 用风力发电代替火力发电 | D. | 把高耗能产业转移到欠发达地区 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com