
【题目】已知二元酸H2A在水中存在以下电离:H2A═H++HA﹣ , HA﹣═H++A2﹣ , 回答下列问题:
(1)Na2A溶液呈性,理由是(用离子方程式表示).
(2)NaHA溶液呈性,理由是 .
(3)0.1mol/L的NaHA溶液的pH=3,则Ka(HA﹣)= .
(4)某温度下,向10mL 0.1mol/L NaHA溶液中加入0.1mol/L KOH溶液V mL至溶液中水的离子积常数Ka=c2(OH﹣),此时溶液呈性,V10 (填“<”“>”或“=”)c(K+)/c(Na+)1(填“<”“>”或“=”),溶液中电荷守恒等式为 .
【答案】
(1)碱; A2﹣+H2O?HA﹣+OH﹣
(2)酸; HA﹣只电离,不发生水解
(3)10﹣5
(4)中;<;<; c(Na+)+c(K+)+c(H+)=c(OH﹣)+c(HA﹣)+2c(A2﹣)
【解析】解:(1)由HA﹣H++A2﹣可知,Na2A为强碱弱酸盐,A2﹣水解显碱性,水解离子反应为A2﹣+H2OHA﹣+OH﹣,
所以答案是:碱;A2﹣+H2OHA﹣+OH﹣;(2)由HA﹣H++A2﹣可知,Na2A为强碱弱酸盐;NaHA为酸式盐,H2A第一步完全电离,所以HA﹣只电离,不发生水解,HA﹣电离生成氢离子,所以溶液显酸性;
所以答案是:酸;HA﹣只电离,不发生水解;(3)0.1mol/L的NaHA溶液的pH=3,HA﹣═H++A2﹣,Ka= ![]() =
= ![]() =10﹣5,;
=10﹣5,;
所以答案是:10﹣5;(4)Kw=c(OH﹣)c(H+)=KW=c2(OH﹣),c(OH﹣)=c(H+),溶液呈中性,NaHA溶液显酸性,某温度下,向10mL 0.1mol/L NaHA溶液中加入0.1mol/L KOH溶液V mL,若恰好反应溶液显碱性,若溶液为中性,需要KOH的量少于NaHA,V<10ml,所以 ![]() 比值小于1,此时溶液中存在的阳离子Na+、K+、H+,阴离子为:OH﹣、HA﹣、A2﹣,溶液中存在电荷守恒c(Na+)+c(K+)+c(H+)=c(OH﹣)+c(HA﹣)+2c(A2﹣),
比值小于1,此时溶液中存在的阳离子Na+、K+、H+,阴离子为:OH﹣、HA﹣、A2﹣,溶液中存在电荷守恒c(Na+)+c(K+)+c(H+)=c(OH﹣)+c(HA﹣)+2c(A2﹣),
所以答案是:中;<;<;c(Na+)+c(K+)+c(H+)=c(OH﹣)+c(HA﹣)+2c(A2﹣).
【考点精析】掌握弱电解质在水溶液中的电离平衡是解答本题的根本,需要知道当弱电解质分子离解成离子的速率等于结合成分子的速率时,弱电解质的电离就处于电离平衡状态;电离平衡是化学平衡的一种,同样具有化学平衡的特征.条件改变时平衡移动的规律符合勒沙特列原理.


 口算心算速算应用题系列答案
口算心算速算应用题系列答案 同步拓展阅读系列答案
同步拓展阅读系列答案科目:高中化学 来源: 题型:
【题目】从某废液(含有Fe2+、Cu2+、Cl﹣)中回收铜并制得纯净的FeCl3溶液.现以制得纯净的FeCl3溶液为原料制取优良的水处理剂高铁酸钾(K2FeO4),其流程如图: 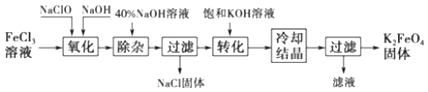
已知:高锰酸钾(K2FeO4)位暗紫色固体,可溶于水.在中性或酸性溶液中逐渐分解,在碱性溶液中稳定.高锰酸钾具有强氧化性.高锰酸钾(K2FeO4)与水作用产生Fe(OH)3 .
(1)检验废液中含有Fe2+选用的试剂是(填化学式);从废液中制得纯净的FeCl3溶液加入的试剂除铁粉外,还需要一种试剂是(填化学式),加入时发生反应的离子方程式为 .
(2)高锰酸钾(K2FeO4)在处理水过程中的作用是和 .
(3)“氧化”过程反应的离子方程式为 .
(4)过滤时需用的玻璃仪器有玻璃棒、烧杯和 , 上述工艺得到的高锰酸钾常含有杂志,可用重结晶法提纯,操作是:将粗产品用溶解,然后 .
(5)用回收的铜为原料可制得粗制CuSO45H2O晶体(含有少量的FeSO47H2O),除去CuSO45H2O晶体中杂志的方法是:向溶液中加入H2O2 , 再调解溶液pH,过滤即可制得纯净的CuSO4溶液,进而制得纯净CuSO45H2O的晶体. 已知:室温时一些物质的Kaq如表:
化学式 | Fe(OH)3 | Fe(OH)2 | Cu(OH)2 |
Kaq | 8.0×10﹣16 | 8.0×10﹣18 | 8.0×10﹣20 |
已知溶液中的离子浓度小于1×10﹣6molL﹣1时就认定沉淀完全.
加双氧水的目的是;若溶液中CuSO4的浓度为3.0molL﹣1 , 通过计算说明此方法可除去粗制CuSO45H2O晶体中FeSO47H2O的理由 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式书写不正确的是
A. 盐酸与Na2SiO3溶液混合: SiO32-+2H+=H2SiO3↓
B. 浓盐酸和二氧化锰共热制取Cl2: MnO2+4H++2Cl- ![]() Mn2++Cl2↑+2H2O
Mn2++Cl2↑+2H2O
C. NO2通入水中: H2O+3NO2=2H++2NO3-+NO
D. 向澄清石灰水中通人过量SO2: SO2+Ca2++2OH-=CaSO4↓+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将0.1mol两种气体烃组成的混合气完全燃烧后得3.36L(标况)CO2和3.6g水蒸气,对于组成判断正确的是( )
A.一定有甲烷
B.一定有乙烯
C.一定有乙炔
D.一定有乙烷
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,向100mL 0.01molL﹣1HA溶液中逐滴加入0.02molL﹣1MOH溶液,图中所示曲线表示混合溶液的pH变化情况(溶液体积变化忽略不计).下列说法中错误的是( ) 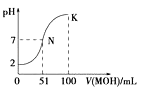
A.HA为一元强酸
B.MOH为一元弱碱
C.N点水的电离程度大于K点水的电离程度
D.K点对应的溶液中:c(MOH)+c(OH﹣)﹣c(H+)=0.01 molL﹣1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NaCl是海水中提取出来的一种重要物质,除食用外,它还是一种工业原料,下列以NaCl为原料的产品是( ) ①烧碱 ②纯碱 ③金属钠 ④氯气 ⑤盐酸.
A.①②③④⑤
B.仅①②③④
C.仅①③④⑤
D.仅①③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,向100mL0.1mol/LNH4HSO4溶液中滴加0.1mol/L的NaOH溶液,所得溶液PH与NaOH溶液体积的关系曲线如图所示,下列说法正确的是( ) 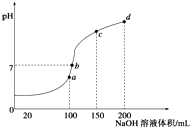
A.a、b、c、d四个点中,水的电离程度最大的是d
B.a点溶液中:c(NH3H2O)+c(H+)═c(OH﹣)
C.b点溶液中:c(Na+)+c(NH4+)═2c(SO42﹣)
D.c点溶液中:c(Na+)═c(SO42﹣)+c(NH4+)+c(NH3H2O)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com