
| A. | 苯分子的核磁共振图表明分子中只存在一种氢原子 | |
| B. | 邻二甲苯没有同分异构体 | |
| C. | 间二甲苯没有同分异构体 | |
| D. | 对二甲苯没有同分异构体 |
分析 A、苯分子的核磁共振图表明分子中只存在一种氢原子,只能说明苯的结构是非常对称的;
B、若苯的结构中存在单、双键交替结构,邻二甲苯的邻位二元取代物有两种;
C、若苯的结构中存在单、双键交替结构,间二甲苯也只有一种;
D、若苯的结构中存在单、双键交替结构,对二甲苯也只有一种.
解答 解:A、苯分子的核磁共振图表明分子中只存在一种氢原子,只能说明苯的结构是非常对称的,而即使苯是单双键交替的结构,苯中的氢原子也全部是等效的,也只有一种,故A错误;
B、若苯的结构中存在单、双键交替结构,邻二甲苯有两种,现在邻二甲苯只有一种,说明苯不是单双键交替的结构,里面的碳碳键完全相同,为平面正六边形结构故B正确;
C、若苯的结构中是单、双键交替结构,间二甲苯仍只有一种,故不能说明苯的结构究竟是不是单双键交替的结构,故C错误;
D、若苯的结构中是单、双键交替结构,对二甲苯仍只有一种,故不能说明苯的结构究竟是不是单双键交替的结构,故D错误.
故选B.
点评 本题考查苯的结构与性质、同分异构体,难度不大,要求学生知识掌握全面,能运用知识分析和解决问题,重在能力的考查.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | Zn(s)+CuSO4(aq)═ZnSO4(aq)+Cu(s)△H=-216kJ•mol-1,则反应物总能量>生成物总能量 | |
| B. | 相同条件下,如果1mol氢原子所具有的能量为E1,1mol 氢分子所具有的能量为E2,则2E1=E2 | |
| C. | 101 kPa时,2H2(g)+O2(g)═2H2O(l)△H=-571.6 kJ•mol-1,则H2的燃烧热为△H=-571.6 kJ•mol-1 | |
| D. | H+(aq)+OH-(aq)═H2O(l)△H=-57.3 kJ•mol-1,则1molNaOH的氢氧化钠固体与含0.5molH2SO4的稀硫酸混合后放出57.3kJ的热量 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1mol的羟基与1mol的氢氧根离子所含电子数均为9NA | |
| B. | 120g NaHSO4固体中含有的离子总数为3NA | |
| C. | 1mol Na被氧化生成Na2O2或NaCl,都失去NA个电子 | |
| D. | 1.0L 1.0mol•L-1的NaNO3水溶液中含有的氧原子数为3NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 维勒用无机物合成了尿素,突破了无机物与有机物的界限 | |
| B. | 门捷列夫在前人的基础上发现了元素周期律 | |
| C. | 煤中含有苯、二甲苯等芳香烃,可以通过先干馏,再分馏分离出苯、二甲苯 | |
| D. | 石油的减压分馏的目的是使沸点高的烃在较低温条件下气化 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | HCl MgCl2 NH4Cl | B. | H2O Na2O CO2 | ||
| C. | CaCl2 ? NaOH H2O | D. | NH3 H2O CO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②③④ | B. | ①②⑤⑥ | C. | ③⑤⑥ | D. | ①③④⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | CO2通入澄清的石灰水中反应的产物 $\frac{n(C{O}_{2})}{n[Ca(OH)_{2}]}$ $\frac{n(C{O}_{2})}{n[Ca(OH)_{2}]}$ | |
| B. | Fe在Cl2中的燃烧产物: $\frac{n(C{l}_{2})}{n(Fe)}$ $\frac{n(C{l}_{2})}{n(Fe)}$ | |
| C. | AlCl3溶液中滴加NaOH后铝的存在形式: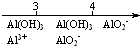 $\frac{n(NaOH)}{n(AlC{l}_{3})}$ $\frac{n(NaOH)}{n(AlC{l}_{3})}$ | |
| D. | 氨水与SO2反应后溶液中的铵盐: $\frac{n(N{H}_{3}{H}_{2}O)}{n(S{O}_{2})}$11 $\frac{n(N{H}_{3}{H}_{2}O)}{n(S{O}_{2})}$11 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com