
【题目】化学与社会、生产、生活紧切相关。下列说法正确的是
A.高纯度的硅单质用于制作光导纤维
B.合金相对于金属单质,其硬度更大、熔沸点更高
C.为了增加食物的营养成分,可以大量使用食品添加剂
D.过氧化钠可以用在潜艇和呼吸面罩中作供氧剂
 手拉手全优练考卷系列答案
手拉手全优练考卷系列答案科目:高中化学 来源: 题型:
【题目】某工业废水中可能含有如下几种阴阳离子:
阳离子 | Fe3+、Al3+、Fe2+、Ba2+、Na+ |
阴离子 | Cl-、CO32-、NO3-、SO42-、S2- |
现对该废水样品进行以下研究:
Ⅰ.向试管中滴加浓盐酸,有少量的无色气体生成,气体遇空气立即变为红棕色;
Ⅱ.若向Ⅰ所得的溶液中加入BaCl2溶液,有白色沉淀生成。
Ⅲ.若向Ⅰ所得的溶液中加入过量的NaOH溶液,有红褐色沉淀生成。过滤后向所得滤液中通入过量的CO2气体,有白色絮状沉淀生成。
根据上述实验,回答下列问题:
(1)该废水中一定含有的阴离子是 _____,一定不含有的阳离子是_____;
(2)写出Ⅰ中产生无色气体的反应的离子方程式:______;
(3)写出Ⅲ中通入过量CO2产生白色絮状沉淀所发生的反应离子方程式:______;
(4)在废水中加入新制氯水,测得溶液中c(Fe3+)=1.0×10-2mol·L-1,c(Al3+)=1.0×10-3mol·L-1。要想使Fe3+完全沉淀(离子浓度为1.0×10-5mol·L-1)而Al 3+不沉淀,则应调节溶液pH范围为______。(已知常温下Fe(OH)3的Ksp=1.0×10-38,Al(OH)3的Ksp=1.0×10-33)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列溶液中,溶质的物质的量浓度不是1 mol/L的是( )
A. 10 g NaOH固体溶解在水中配成250 mL溶液
B. 将80 g SO3溶于水并配成1 L的溶液
C. 将0.5 mol/L的NaNO3溶液100 mL加热蒸发掉50 g水的溶液
D. 标况下,将22.4 L氯化氢气体溶于水配成1 L溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】合成氨工业对国民经济和社会发展具有重要的意义。对于密闭容器中的反应:N2(g)+3H2(g)![]() 2NH3(g)(正反应为放热反应),673K、30MPa下,n(NH3)和n(H2)随时间 t变化的关系如图所示。下列叙述中,正确的是( )
2NH3(g)(正反应为放热反应),673K、30MPa下,n(NH3)和n(H2)随时间 t变化的关系如图所示。下列叙述中,正确的是( )

A. 点a的正反应速率比点b的小
B. 点c处正反应速率和逆反应速率相等
C. 点d (t1时刻) 和点 e (t2时刻) 处n(N2)相同
D. 在t2时刻,正反应速率大于逆反应速率
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.下列物质中:
(1)互为同分异构体的有_______ (2)互为同素异形体的有_______
(3)属于同位素的有__________ (4)属于同一种物质的有______。(填序号)
①液氯和氯气 ②白磷和红磷 ③ 和
和![]() ④3717Cl和3517Cl⑤(CH3)2CHCH3和CH3(CH2)2CH3 ⑥
④3717Cl和3517Cl⑤(CH3)2CHCH3和CH3(CH2)2CH3 ⑥![]() 和
和 ⑦CH4和CH3CH2CH3
⑦CH4和CH3CH2CH3
Ⅱ.现有6种物质:①MgCl2 ②HCl ③SO2 ④K2CO3 ⑤CaO ⑥NaOH
请根据下列标准,对上述物质进行分类(填序号):
(1)属于共价化合物是_______。
(2)含共价键的离子化合物是______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用黄铜矿(主要成分是CuFeS2)生产粗铜的反应原理如下:
![]()
(1)已知在反应①、②中均生成相同的气体分子,该气体具有漂白性。请分别写出反应①、②的化学方程式________________、__________________。
(2)基态铜原子的核外电子排布式为____________,硫、氧元素相比,第一电离能较大的是______。
(3)反应①和②生成的气体分子的中心原子的杂化类型是______,分子的空间构型是______。
(4)C、Si为同一主族的元素,CO2和SiO2化学式相似,但结构和性质有很大不同。CO2中C与O原子间形成σ键和π键,SiO2中Si与O原子间不形成上述π键。从原子半径大小的角度分析,为何C、O原子间能形成,而Si、O原子间不能形成上述π键________________。
(5)Cu2O的晶胞结构如图所示,该晶胞的边长为a cm,则Cu2O的密度为__________g·cm-3(用NA表示阿伏加德罗常数的数值)。
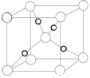
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在反应3S +6KOH=K2SO3 +2K2S +3H2O 中,作还原剂和作氧化剂的硫原子个数比为
A.1:2 B.2:1 C.1:1 D.3:2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下,下列叙述不是可逆反应A(g)+3B(g) ![]() 2C(g)达到平衡的标志的是:①C的生成速率与C的分解速率相等;②单位时间内有a mol A生成的同时生成3a mol B;③A、B、C的浓度不再变化;④容积不变的密闭容器中混合气体的总压强不再变化;⑤混合气体的物质的量不再变化;⑥单位时间消耗a mol A,同时生成3a mol B;⑦A、B、C的分子数目之比为1∶3∶2。
2C(g)达到平衡的标志的是:①C的生成速率与C的分解速率相等;②单位时间内有a mol A生成的同时生成3a mol B;③A、B、C的浓度不再变化;④容积不变的密闭容器中混合气体的总压强不再变化;⑤混合气体的物质的量不再变化;⑥单位时间消耗a mol A,同时生成3a mol B;⑦A、B、C的分子数目之比为1∶3∶2。
A. ②⑤ B. ①③ C. ②⑦ D. ⑤⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:CH3CH2CH2CH2OH→CH3CH2CH2CHO
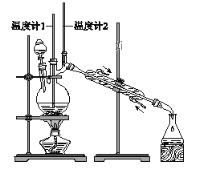
利用下图装置用正丁醇合成正丁醛。相关数据如下:
物质 | 沸点/℃ | 密度/(g·cm-3) | 水中溶解性 |
正丁醇 | 117.2 | 0.8109 | 微溶 |
正丁醛 | 75.7 | 0.8017 | 微溶 |
下列说法中,不正确的是( )
A. 为防止产物进一步氧化,应将酸化的Na2Cr2O7溶液逐滴加入正丁醇中
B. 向获得的粗正丁醛中加入少量金属钠,检验其中是否含有正丁醇
C. 反应结束,将馏出物倒入分液漏斗中,分去水层,粗正丁醛从分液漏斗上口倒出
D. 当温度计1示数为90~95℃,温度计2示数在76℃左右时,收集产物
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com