
����Ŀ��NaOH��Һ�����ڶ�������Ĵ�����
(1)CO2���������壬����NaOH��Һ���յõ�Na2CO3��NaHCO3��
��Na2CO3�׳ƴ����CO32��ˮ���ʹ��ˮ��Һ�ʼ��ԣ�д��CO32����һ��ˮ������ӷ���ʽ_________����֪25��ʱ��CO32����һ��ˮ���ƽ�ⳣ��Kh=2��10��4mol/L������Һ��c��HCO3������c��CO32����=20��1 ʱ����Һ��pH=_____��
����ĭ�������ͨ��װ��NaHCO3 ��Һ��Al2(SO4)3��Һ����д����������Һ���ʱ�����ӷ�Ӧ����ʽ__________��
(2)������Ũ���ᷴӦ������NO2����NaOH��Һ���գ���Ӧ����ʽΪ��2NO2+2NaOH=NaNO3+NaNO2+H2O����0.2molNaOH��ˮ��Һ��0.2mol NO2ǡ����ȫ��Ӧ��1L��ҺA����ҺBΪ0��lmolL��1CH3COONa��Һ����������Һ��c��NO3������c��NO2������c��CH3COO�����ɴ�С��˳��Ϊ___________����֪HNO2�ĵ��볣��Ka=7.1��10��4molL��1��CH3COOH�ĵ��볣��Ka=1.7��10��5molL��1������ʹ��ҺA����ҺB�� pH��ȵķ�����_____��
A������ҺA�м�����NaOH B������ҺA�м�����ˮ
C������ҺB�м�����NaOH D������ҺB�м�����ˮ
(3)�����е�SO2���������꣬����������������Һ���ա�����SO2�Ĺ����У���Һ��H2SO3��HSO3����SO32��������ռ���ʵ���������a����pH�仯�Ĺ�ϵ��ͼ��ʾ��
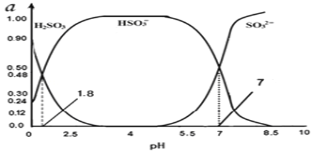
��ͼ��pH=7ʱ����Һ������Ũ�ȹ�ϵ��ȷ����___��
A��c��Na+����2c��SO32������c��HSO3����
B��c��Na+��=c��SO32����+c��HSO3����+c��H2SO3��
C��c��OH����=c��H+��+c��H2SO3��+c��HSO3����
D��c��Na+����c��HSO3������c��SO32������c��H+��=c��OH����
��������ͼ�����ݣ���ӦH2SO3![]() H++ HSO3����ƽ�ⳣ������ֵ____��
H++ HSO3����ƽ�ⳣ������ֵ____��
���𰸡�CO32��+H2O ![]() HCO3��+OH�� 9 3HCO3��+Al3+=Al(OH)3��+3CO2�� c��NO3������c��NO2������c��CH3COO���� AD A 10-1.8
HCO3��+OH�� 9 3HCO3��+Al3+=Al(OH)3��+3CO2�� c��NO3������c��NO2������c��CH3COO���� AD A 10-1.8
��������
(1)��CO32-ˮ���ʹ��ˮ��Һ�ʼ��ԣ���CO32-��һ��ˮ������ӷ���ʽΪ��CO32-+H2OHCO3-+OH-��ˮ�ⳣ��Kh= ������Һ��c(HCO3-)��c(CO32-)=20��1ʱ������ˮ�ⳣ������c(OH-)���ɸ���ˮ�����ӻ�Kw����c(H+)������pH=-lgc(H+)���㣻
������Һ��c(HCO3-)��c(CO32-)=20��1ʱ������ˮ�ⳣ������c(OH-)���ɸ���ˮ�����ӻ�Kw����c(H+)������pH=-lgc(H+)���㣻
��Al2(SO4)3��NaHCO3���ʱ����ٽ�ˮ��������������������������̼���壻
(2)��ҺA��NaNO3��NaNO2��Ũ�Ⱦ�Ϊ0.1mol/L��HNO2��CH3COOH��Ϊ���ᣬ�ɵ��볣����֪CH3COOH����С��HNO2�����ԣ���Һ�д��������ˮ��̶ȴ��������������ˮ��̶ȣ���ҺB���Դ���A��Һ��
(3)��A���ɵ���غ��֪��c(H+)+c(Na+)�T2c(SO32-)+c(HSO3-)+c(OH-)��������Һ��c(H+)�Tc(OH-)����c(Na+)�T2c(SO32-)+c(HSO3-)������c(Na+)��2c(SO32-)����ͼ��֪pH=7ʱ��c(SO32-)=c(HSO3-)����c(Na+)��2c(SO32-)��c(HSO3-)����A ��ȷ��
B���ɵ���غ��֪��c(H+)+c(Na+)�T2c(SO32-)+c(HSO3-)+c(OH-)��������Һ��c(H+)�Tc(OH-)����c(Na+)�T2c(SO32-)+c(HSO3-)��c(SO32-)��c(H2SO3)����B����
C��pH=7ʱ��c(H+)=c(OH-)��
D��HSO3-����̶ȴ���ˮ��̶ȵ�����Һ�����ԣ���Ϊ������������Ӽ��ܵ�������ˮ�⣬������Һ�д���H2SO3��SO32-����NaHSO3��Һ�д��ڵ���غ�������غ㣬���ݵ���غ�������غ��жϣ�
��H2SO3![]() H++ HSO3������ͼ�����ݣ�pH=1.8ʱ��c(H2SO3 )=c(HSO3- )����Ka�ı���ʽ��֪��H2SO3�ĵ�һ������ƽ�ⳣ��Ka1��c(H+)=10-1.8���ɴ˷������
H++ HSO3������ͼ�����ݣ�pH=1.8ʱ��c(H2SO3 )=c(HSO3- )����Ka�ı���ʽ��֪��H2SO3�ĵ�һ������ƽ�ⳣ��Ka1��c(H+)=10-1.8���ɴ˷������
(1)��CO32��ˮ���ʹ��ˮ��Һ�ʼ��ԣ�CO32����һ��ˮ������ӷ���ʽΪ��CO32��+H2OHCO3��+OH����ˮ�ⳣ��Kh=2��10��4������Һ��c(HCO3-)��c(CO32��)=20��1ʱ��c(OH��)=10��5mol/L����ˮ�����ӻ�Kw��֪��c(H+)=10��9mol/L������pH=��lg10��9=9��
��Al2(SO4)3��NaHCO3���ʱ����ٽ�ˮ��������������������������̼���壬���ӷ���ʽΪAl3++3HCO3���TAl(OH)3��+3CO2����
(2)0.2mol NaOH��ˮ��Һ��0.2mol NO2ǡ����ȫ��Ӧ��1L��ҺA����2NO2+2NaOH�TNaNO3+NaNO2+H2O���õ���ҺA��NaNO3���ʵ���Ũ��Ϊ0.1mol/L��NaNO2���ʵ���Ũ��Ϊ0.1mol/L����ҺBΪ0.1molL��1��CHCOONa��Һ�� HNO2�ĵ��볣��Ka=7.1��10��4molL��1��CH3COOH�ĵ��볣��Ka=1.7��10��5molL��1��˵��CH3COOH����С��HNO2�����ԣ���Һ�д��������ˮ��̶ȴ��������������ˮ��̶ȣ���ҺB���Դ���A��Һ������Һ��c(NO3��)��c(NO2��)��c(CH3COO��)�ɴ�С��˳��Ϊc(NO3��)��c(NO2��)��c(CH3COO��)��
A������ҺA�м�����NaOH��������ԣ����Ե�����ҺpH��ȣ���A��ȷ��
B����ҺB���Դ���A��Һ������ҺA�м�����ˮ��ϡ����Һ�����Լ��������ܵ�����ҺpH��ȣ���B����
C����ҺB���Դ���A��Һ������ҺB�м�����NaOH����ҺpH����C����
D������ҺB�м�����ˮ��ϡ����Һ���Լ��������Ե�����ҺpH��ȣ���D��ȷ��
�ʴ�ΪAD��
(3)��A���ɵ���غ��֪��c(H+)+c(Na+)�T2c(SO32��)+c(HSO3��)+c(OH��)��������Һ��c(H+)�Tc(OH��)����c(Na+)�T2c(SO32��)+c(HSO3��)������c(Na+)��2c(SO32��)������ͼ��֪pH=7ʱ��c(SO32��)=c(HSO3��)����c(Na+)��2c(SO32��)��c(HSO3��)����A ��ȷ��
B���ɵ���غ��֪��c(H+)+c(Na+)�T2c(SO32��)+c(HSO3��)+c(OH��)��������Һ��c(H+)�Tc(OH��)����c(Na+)�T2c(SO32��)+c(HSO3��)��c(SO32��)��c(H2SO3)����B����
C��pH=7ʱ��c(H+)=c(OH��)����C����
D����ͼ��֪pH=7ʱ��c(SO32��)=c(HSO3��)����D����
�ʴ�ΪA��
��������ĵ�һ�����뷽��ʽΪ��H2SO3![]() H++HSO3��������ͼ���֪��pH=1.8ʱ��c(H2SO3 )=c(HSO3- )����Ka=
H++HSO3��������ͼ���֪��pH=1.8ʱ��c(H2SO3 )=c(HSO3- )����Ka= ��֪��H2SO3�ĵ�һ������ƽ�ⳣ��Ka1��c(H+)=10-1.8��
��֪��H2SO3�ĵ�һ������ƽ�ⳣ��Ka1��c(H+)=10-1.8��


 â���̸������Ծ�ϵ�д�
â���̸������Ծ�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪ij�¶���0.1 mol/L��NaHB(ǿ�����)��Һ��c(H��)>c(OH��)�������й�ϵһ����ȷ����(����)
A. c(Na��)��c(HB��)��2c(B2��)��c(OH��)
B. c(Na��)��0.1 mol/L��c(B2��)
C. HB����ˮ�ⷽ��ʽΪHB����H2O![]() B2����H3O��
B2����H3O��
D. �ڸ��ε���Һ�У�����Ũ�ȴ�С˳��Ϊc(Na��)>c(HB��)>c(B2��)>c(OH��)>c(H��)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��![]() Ϊ��Ԫ���ᣬ
Ϊ��Ԫ���ᣬ![]() ��
��![]() ����
����![]() ��Һ��
��Һ��![]() ����������NaOH��Һ�ζ�
����������NaOH��Һ�ζ�![]() ��Һ���յ㡣�ζ����̵õ���������Һ���������ʵ���Ũ�ȹ�ϵһ����ȷ����( )
��Һ���յ㡣�ζ����̵õ���������Һ���������ʵ���Ũ�ȹ�ϵһ����ȷ����( )
A.![]() ��Һ��
��Һ��![]()
B.![]() ����Һ��
����Һ��![]()
C.![]() ����Һ��
����Һ��![]()
D.![]() ����Һ��
����Һ��![]()
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪��25��ʱ��Kb(NH3��H2O)=1.8��10-5�����¶�������0.100mol��L-1�İ�ˮ�ζ�10.00mL0.100mol��L-1��һԪ��HA����Һ���ζ������м��백ˮ�����(V)����Һ��lg![]() �Ĺ�ϵ����ͼ��ʾ������˵������ȷ����
�Ĺ�ϵ����ͼ��ʾ������˵������ȷ����

A. a=10 B. HAΪǿ��
C. 25��ʱ��NH4+��ˮ��ƽ�ⳣ��Ϊ![]() ��10-9 D. �����백ˮ�����V=20mLʱ����Һ�д���c(NH4+)>c(A-)
��10-9 D. �����백ˮ�����V=20mLʱ����Һ�д���c(NH4+)>c(A-)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��(1)�״�![]() ����Ҫ���ܼ������ȼ�ϣ���ҵ����CO��H2��һ���������Ʊ�
����Ҫ���ܼ������ȼ�ϣ���ҵ����CO��H2��һ���������Ʊ�![]() �ķ�Ӧ��
�ķ�Ӧ��![]() �������Ϊ1L�ĺ����ܱ������У���2molCO��
�������Ϊ1L�ĺ����ܱ������У���2molCO��![]() ��һ�������·���������Ӧ�����
��һ�������·���������Ӧ�����![]() ��
��![]() ��Ũ����ʱ��仯��ͼ��ʾ��
��Ũ����ʱ��仯��ͼ��ʾ��

�ٴӷ�Ӧ��ʼ��5min����һ����̼��ʾ��ƽ����Ӧ��������CO��=______��
������˵����ȷ����______��
A.�ﵽƽ��ʱ��![]() ��ת����Ϊ
��ת����Ϊ![]()
B.5min�������л�������ƽ����Է����������ٸı�
C.�ﵽƽ����ٳ��백������Ӧ���ʼ�С
D.2minǰ��������>�����棩��2min����������<�����棩
(2)һ���¶��£���![]() ��
��![]() �������1��2�����ܱ������з�����Ӧ��
�������1��2�����ܱ������з�����Ӧ��
![]() ���ﵽƽ��ʱ
���ﵽƽ��ʱ![]() ���������Ϊ
���������Ϊ![]() ���÷�Ӧ��ƽ�ⳣ��
���÷�Ӧ��ƽ�ⳣ��![]() ______��
______��
(3)̼��ˮ������Ӧ��ȡ![]() ����ط�Ӧ���£�
����ط�Ӧ���£�
��![]()
��![]()
��![]()
�ټ��㷴Ӧ![]() ��
��![]() ______
______![]()
�ڶ��ڿ��淴Ӧ![]() ����ȡ���´�ʩ�������
����ȡ���´�ʩ�������![]() ���ʵ���______��
���ʵ���______��
A.������ϵ���¶�
B.ѹ�����������
C.����CaO����
D.ѡ���ʵ��Ĵ���
(4)�Լ״�Ϊȼ�ϣ�![]() Ϊ��������KOH��ҺΪ�������Һ�����Ƴ�ȼ�ϵ��
Ϊ��������KOH��ҺΪ�������Һ�����Ƴ�ȼ�ϵ��![]() �缫����Ϊ���Ե缫
�缫����Ϊ���Ե缫![]() ����KOH��Һ������д����ȼ�ϵ�ظ����ĵ缫��Ӧʽ��______��
����KOH��Һ������д����ȼ�ϵ�ظ����ĵ缫��Ӧʽ��______��
(5)����20mL![]() ������
������![]() ��Һ����μ���һ��Ũ�ȵ��ռ���Һ����û����Һ���¶ȱ仯��ͼ��ʾ�������й�˵����ȷ����______
��Һ����μ���һ��Ũ�ȵ��ռ���Һ����û����Һ���¶ȱ仯��ͼ��ʾ�������й�˵����ȷ����______

�ٸ��ռ���Һ��Ũ��Ϊ![]()
�ڸ��ռ���Һ��Ũ��Ϊ![]()
��![]() �ĵ���ƽ�ⳣ����b��
�ĵ���ƽ�ⳣ����b��![]() ��
��
�ܴ�b�㵽c�㣬�����Һ��һֱ���ڣ�c(Na+)>c(NO2-)>c(OH-)>c(H+)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij�¶��£����ܱ�������SO2��O2��SO3������̬���ʽ�����ѧƽ��ı������Է�Ӧ2SO2(g)��O2(g)2SO3(g)����H<0�������淴Ӧ���ʵ�Ӱ����ͼ��ʾ��

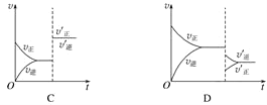
(1)�Ӵ����Է�Ӧ����Ӱ���ͼ����__________(����ĸ����ͬ)��ƽ��__________�ƶ���
(2)�����¶ȶԷ�Ӧ����Ӱ���ͼ����__________��ƽ����__________�����ƶ���
(3)����Ӧ��������Է�Ӧ����Ӱ���ͼ����__________��ƽ����__________�����ƶ���
(4)����O2��Ũ�ȶԷ�Ӧ����Ӱ���ͼ����__________��ƽ����__________�����ƶ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����10L�ܱ������У�A��B��C������̬���ʹ����˿��淴Ӧ����ϵ��һ�������£�A��B��C�����������ʵ���![]() ��ʱ��
��ʱ��![]() �Ĺ�ϵ��ͼһ��ʾ��C�İٷֺ���
�Ĺ�ϵ��ͼһ��ʾ��C�İٷֺ���![]() ���¶�
���¶�![]() �Ĺ�ϵ��ͼ����ʾ�����з����������
�Ĺ�ϵ��ͼ����ʾ�����з����������

A.![]() ʱ��A��ƽ����Ӧ����Ϊ
ʱ��A��ƽ����Ӧ����Ϊ![]()
B.ͼ����![]() ��
��![]() ��Ӧ�����ϵĵ㶼���ڻ�ѧƽ��״̬
��Ӧ�����ϵĵ㶼���ڻ�ѧƽ��״̬
C.��![]() ��
��![]() �仯ʱ��
�仯ʱ��![]()
D.�÷�Ӧ������ӦΪ���ȷ�Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ʵ�鷽�������ﵽ��ӦĿ�ĵ���
A | B | C | D | |
Ŀ�� | �Ƚ�̼�����̼�����ˮ��̶� | �о�Ũ�ȶԻ�ѧƽ���Ӱ�� | �Ƚϲ�ͬ�����Ի�ѧ��Ӧ���ʵ�Ӱ�� | �Ƚ�̼�ᡢ��������������ǿ�� |
ʵ�鷽�� |
|
|
|
|
A. AB. BC. CD. D
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij�¶�ʱ��BaSO4��ˮ�еij����ܽ�ƽ��������ͼ��ʾ������˵����ȷ����

A. ����Na2SO4��ʹ��Һ��a��䵽b��
B. ͨ����������ʹ��Һ��d��䵽c��
C. d����BaSO4��������
D. a���Ӧ��Ksp����c���Ӧ��Ksp
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com