

| ||
| ||
| ||
| 950℃--970℃Na3AlF6 |
| ||
| 950℃--970℃Na3AlF6 |


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
| a |
| 4 |
| A、2:1 | B、3:1 |
| C、4:1 | D、9:2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 族 周期 |
IA | 0 | ||||||
| 1 | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | ||
| 2 | ① | ② | ③ | |||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ||
查看答案和解析>>
科目:高中化学 来源: 题型:
| 浓硫酸 |
| s |
查看答案和解析>>
科目:高中化学 来源: 题型:

| 沉淀物 | Fe(OH)3 | Cu(OH)2 | Mg(OH)2 |
| pH | 3.2 | 6.7 | 12.4 |
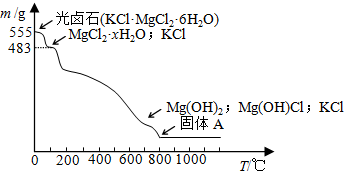
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、海水是一个巨大的宝藏,如氯、溴、碘、硫、钠、钾等元素主要来自于海水 |
| B、近期媒体报道的某白酒中的增塑剂是对人体健康有害的物质 |
| C、以NO和NO2为主的氮氧化物是形成光化学烟雾和酸雨的一个重要原因 |
| D、高纯度的二氧化硅广泛用于制作光导纤维 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com