
|
平衡:如化学平衡、溶解平衡、电离平衡.下列不存在平衡的是(不考虑水的电离平衡) | |
| [ ] | |
A. |
稀醋酸水溶液中 |
B. |
氢氧化钙悬浊液中 |
C. |
二氧化硫与氧气反应的混合物中 |
D. |
稀氯化钠水溶液中 |
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:阅读理解
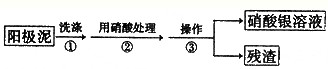
| 编号 | 常温下反应 | 化学平衡常数 |
| 反应1 | Au+6HNO3 Au(NO3)3+3NO2↑+3H2O Au(NO3)3+3NO2↑+3H2O |
<10-5 |
| 反应2 | Au3++Cl-  [AuCl4]- [AuCl4]- |
>105 |
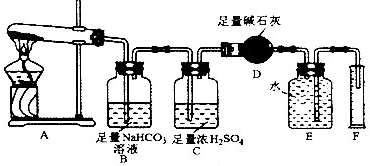
| ||
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
 化学学科中的平衡理论主要包括:化学平衡、电离平衡、水解平衡和溶解平衡四种,且均符合勒夏特列原理.请回答下列问题:
化学学科中的平衡理论主要包括:化学平衡、电离平衡、水解平衡和溶解平衡四种,且均符合勒夏特列原理.请回答下列问题:| c(CH3OH) |
| c(CO)c2(H2) |
| c(CH3OH) |
| c(CO)c2(H2) |
| 2nB |
| 3tB |
| 2nB |
| 3tB |
| O | 2- 3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 研究化学反应原理对于生产、生活及环境保护具有重要意义.
研究化学反应原理对于生产、生活及环境保护具有重要意义.查看答案和解析>>
科目:高中化学 来源: 题型:
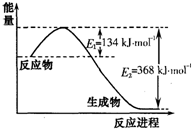 氮是地球上含量丰富的一种元素,氮及其化合物在工农业生产、生活中有着重要作用.请回答下列问题:
氮是地球上含量丰富的一种元素,氮及其化合物在工农业生产、生活中有着重要作用.请回答下列问题:| t/K | 298 | 398 | 498 | … |
| K/(mol?L-1)-2 | 4.1×106 | K1 | K2 | … |
查看答案和解析>>
科目:高中化学 来源:2010年安徽省高考化学练习试卷(一)(解析版) 题型:填空题
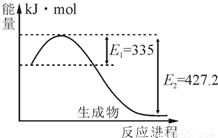
 2NH3,则在电化学合成氨的过程中,阴极反应式为 .
2NH3,则在电化学合成氨的过程中,阴极反应式为 .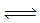 2NH3(g),△H<0,其化学平衡常数K与t的关系如下表:、C(H2)、C(NH3)分别为平衡浓度)
2NH3(g),△H<0,其化学平衡常数K与t的关系如下表:、C(H2)、C(NH3)分别为平衡浓度)| t/K | 298 | 398 | 498 | … |
| K/-2 | 4.1×106 | K1 | K2 | … |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com