(2011?太原二模)[化学-化学与技术]硫酸工业生产应考虑综合经济效益问题.
(1)若从下列四个城市中选择一处新建一座硫酸厂,你认为厂址宜选在
C
C
的郊区(填标号);
A.有丰富黄铁矿资源的城市
B.风光秀丽的旅游城市
C.消耗硫酸甚多的工业城市
D.人口稠密的文化、商业中心城市
(2)CuFeS
2是黄铁矿的另一成分,煅烧时CuFeS
2转化为CuO、Fe
2O
3 和SO
2,该反应的化学方程式为
4CuFeS
2+13O
24CuO+2Fe
2O
3+8SO
24CuFeS
2+13O
24CuO+2Fe
2O
3+8SO
2.
(3)在硫酸工业制法中,下列生产操作与说明生产操作的主要原因二者都是正确的是
D
D
.
A.黄铁矿燃烧前需要粉碎,因为大块的黄铁矿不能在空气中燃烧
B.从沸腾炉出来的炉气需净化,因为炉气中二氧化硫会与杂质反应
C.二氧化硫氧化为三氧化硫时需使用催化剂,这样可以提高二氧化硫的转化率
D.三氧化硫用98.3%的浓硫酸吸收,目的是防止形成酸雾,以提高三氧化硫的吸收效率
(4)由硫酸厂沸腾炉排出的矿渣中含有Fe
2O
3、CuO、CuSO
4(由CuO与SO
3 在沸腾炉中化合而成),其中硫酸铜的质量分数随沸腾炉温度不同而变化(见下表)
| 沸腾炉温度/℃ |
600 |
620 |
640 |
660 |
| 炉渣中CuSO4的质量分数/% |
9.3 |
9.2 |
9.0 |
8.4 |
已知CuSO
4 在低于660℃时不会分解,请简要分析上表中CuSO
4的质量分数随温度升高而降低的原因
SO2转化为SO3是正反应放热的可逆反应,随温度升高,平衡左移,SO3物质的量减少,所以CuSO4的量减少
SO2转化为SO3是正反应放热的可逆反应,随温度升高,平衡左移,SO3物质的量减少,所以CuSO4的量减少
.






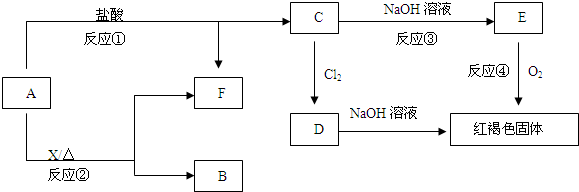
 类反应的名称是
类反应的名称是