
| ѡ�� | ���� | ������ | ���ӹ����жϼ���Ӧ�����ӷ���ʽ |
| A | �μӰ�ˮ | Na+��Al3-��Cl-��NO3- | ���ܴ������棬 Al3++3OH-�TAl��OH��3�� |
| B | ��ˮ�������H+Ũ��Ϊ1��10-12mol?L-1 | NH4+��Na+��NO3-��Cl- | һ���ܴ������棬NH4++H2O?MH3?H2O+H+ |
| C | pH=1����Һ | Fe2+��Al3+��SO42-��MnO4- | ���ܴ������棬5Fe2++MnO4-+8H+�TMn2++5Fe3++4H2O |
| D | ͨ������SO2���� | K+��Na+��ClO-��SO42- | ���ܴ������棬2ClO-+SO2+H2O�T2HClO+SO32- |
| A��A | B��B | C��C | D��D |



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A�������غ㡢�����غ㡢����غ� |
| B�������غ㡢�����غ㡢����غ� |
| C�������غ㡢����غ㡢�����غ� |
| D������غ㡢�����غ㡢�����غ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��32g O2���庬�е���ԭ����ΪNA |
| B��2L 0.3mol/L Na2SO4��Һ�к���Na+Ϊ0.6NA |
| C��27g����ȫ��Ӧ��ʧȥ�ĵ�����Ϊ3NA |
| D��11.2L���������ķ�����Ϊ0.5NA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
A��1mol��˾ƥ�֣�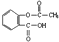 ����������NaOH��Һ��Ӧ������NaOH�������ʵ���Ϊ2mol ����������NaOH��Һ��Ӧ������NaOH�������ʵ���Ϊ2mol |
| B�����͡����͵ȿ�������ֲ������Ҫ�ɷֶ���������������ȡ��ˮ�е��� |
| C��������ͱ���������ˮ����������4�ֶ��� |
D����ϵͳ��������������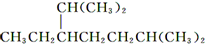 ������Ϊ2��5��������� ������Ϊ2��5��������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A����AΪþ��XΪ��������Bһ������ |
| B����BΪH2O2����X��Y�в�������O2 |
| C����A��B��X��Y��Ϊ������÷�Ӧһ�����ڸ��ֽⷴӦ |
| D�����÷�ӦΪ�û���Ӧ��A��XΪ���ʣ���A��X��ӦԪ�ؿ�����ͬһ���ڣ�Ҳ������ͬһ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��SiX4��ˮ�� |
| B��SiX4�ǹ��ۻ����� |
| C��NaX��ˮ�� |
| D��NaX���۵�һ�����SiX4 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
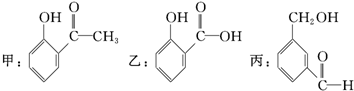
| A�����ߺ��еĹ����ŵ�������ͬ |
| B���Һͱ��е�-OH������ͬ |
| C�����һ�Ϊͬ���칹�� |
| D���ͱ���Ϊͬ���칹�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
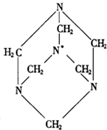 �����μ��İ���һ����Ҫ�Ļ���ԭ�ϣ���ṹʽ��ͼ��ʾ�����й��ڻ����μ��İ����ӽṹ����������ȷ���ǣ�������
�����μ��İ���һ����Ҫ�Ļ���ԭ�ϣ���ṹʽ��ͼ��ʾ�����й��ڻ����μ��İ����ӽṹ����������ȷ���ǣ�������| A�����������е�N��Cԭ�ӹ��� |
| B���ṹʽ�д�*��Nԭ�Ӵ��ڷ��ӵ����� |
| C�������к���3����ͬ��C��N�������е���Ԫ�� |
| D�����ӷ����е�4��Nԭ�ӿɹ���һ���������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| ��ѧʽ | NH3?H2O | CH3COOH | HCN | H2CO3 |
| ����ƽ�ⳣ����25�棩 | 1.8��l0-5 | 1.8��l0-5 | 4.9��l0-10 | K1=4.3��l0-7�� K2=5.6��l0-11 |
| A��0.1mol?L-1 CH3COONa��Һ�Լ��ԣ�0.1mol?L-1 CH3COONH4��Һ������ |
| B�������ʵ���Ũ�ȵ�NaHCO3��NaCN��Һ��ǰ����Һ��ˮ�ĵ���̶ȴ� |
| C��NaCN+H2O+CO2��������=HCN+NaHCO3 |
| D������3�ֵ������pH������Һ���ֱ��ˮϡ�ͺ�pH����ȣ�������м���ˮ��������� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com