
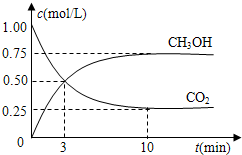
 在体积为1L的密闭容器中(体积不变),充入1mol CO2和3mol H2,一定条件下发生如下反应:CO2(g)+3H2(g)?CH3OH(g)+H2O(g)测得CO2和CH3OH(g)的浓度随时间变化如图.
在体积为1L的密闭容器中(体积不变),充入1mol CO2和3mol H2,一定条件下发生如下反应:CO2(g)+3H2(g)?CH3OH(g)+H2O(g)测得CO2和CH3OH(g)的浓度随时间变化如图.| △c |
| △t |
| 0.75mol/L |
| 10min |


科目:高中化学 来源: 题型:
| A、滴加甲基橙试剂显红色的溶液中:Na+、Fe2+、Cl-、NO3- |
| B、水电离出的c(H+)=10-12mol/L的溶液中:K+、Na+、SO4 2-、AlO2- |
| C、能与铝反应生成氢气的溶液中:Mg2+、Na+、Cl-、NO3- |
| D、滴入KSCN显血红色的溶液中:NH4+、Mg2+、SO42-、Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 容器 | 实验1 | 实验2 | 实验3 |
| 反应物投入量(始态) | 1mol N2、3mol H2 | 2mol NH3 | 4mol NH3 |
| NH3的平衡浓度/mol?L-1 | cl | c2 | c3 |
| 反应的能量变化 | 放出a kJ | 吸收b kJ | 吸收c kJ |
| 体系压强( Pa) | p1 | p 2 | p3 |
| 反应物转化率 | α1 | α2 | α3 |
| A、a+b=92.4 |
| B、2cl>c3 |
| C、2p2<p3 |
| D、(α1+α3)<1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、参加反应物质的性质是决定化学反应速率的主要因素 |
| B、光是影响某些化学反应速率的外界条件之一 |
| C、对于一个化学反应,既可以用反应物表示其化学反应速率,也可以用生成物表示其化学反应速率 |
| D、不管什么反应,增大浓度,或加热或加压,或使用催化剂,都可以加快反应速率 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 熔点 | 沸点 | 状态 | |
| 苯 | 5.51℃ | 80.1 | 液体 |
| 硝基苯 | 5.7℃ | 210.9℃ | 液体 |
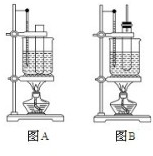
查看答案和解析>>
科目:高中化学 来源: 题型:

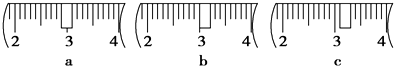
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
2- 4 |
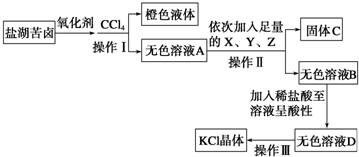
2- 4 |

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com