
 .
.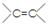 两边基团换位的反应.如两个丙烯分子进行烯烃换位,生成丁烯和乙烯.
两边基团换位的反应.如两个丙烯分子进行烯烃换位,生成丁烯和乙烯.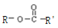 +H2O
+H2O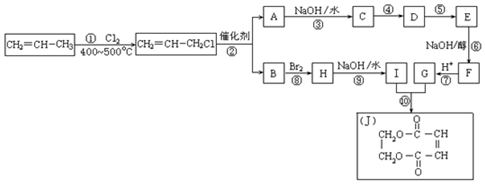
 .
.分析 (1)丙烯中含有碳碳双键,在一定条件下能发生加聚反应生成聚丙烯;
(2)对比两种方法可知:方法②比方法①原料丰富,能耗低,且方法①使用了有毒气体HCN而②没有,减少了污染,据此进行判断;
(3)丙烯与氯气在加热条件下发生取代反应生成CH2=CHCH2Cl,由反应信息可知,CH2=CHCH2Cl在催化剂条件下发生复分解反应生成CH2=CH2、ClCH2CH=CHCH2Cl,A在氢氧化钠水溶液、加热条件下发生反应生成C,故A为ClCH2CH=CHCH2Cl,B为CH2=CH2.B与溴发生加成反应生成H为BrCH2CH2Br,H在氢氧化钠水溶液、加热条件下发生取代反应生成I为HOCH2-CH2OH.A在氢氧化钠水溶液、加热条件下发生反应生成C为HOCH2CH=CHCH2OH,由J的结构可知,G为HOOC-CH=CH-COOH,由转化关系可知,结合反应④是C与HCl加成生成D,保护C=C不被氧化,D再氧化可得E,故D为HOCH2CH2CHClCH2OH,E为
解答 解:(1)丙烯中含有碳碳双键,在一定条件下能发生加聚反应生成聚丙烯,反应方程式为 ,
,
故答案为: ;
;
(2)根据反应原理可知,方法2比方法1原料比较丰富,能源消耗低,成本低,并且方法①中使用了有毒的HCN,而方法2比方法1降低了有毒气体的使用,减少了污染;
故答案为:生产成本低(原料易得、节能),无毒性;
(3)(i)反应①是CH2=CHCH3与氯气发生取代反应生成CH2=CHCH2Cl,反应⑥是卤代烃发生的消去反应,故答案为:取代反应;消去反应;加成反应;
(ii)反应④是C与HCl加成D,设计这一步反应的目的是保护分子中碳碳双键不被氧化,D再氧化可得E,故D为HOCH2CH2CHClCH2OH,E为

(iii)由上述分析可知,C的结构简式为HOCH2CH=CHCH2OH,属于酯类且属于甲酸酯的所有同分异构体的结构简式为HCOOCH2CH2CH3,HCOOCH(CH3)2,故答案为:HCOOCH2CH2CH3,HCOOCH(CH3)2.
点评 本题考查有机方程式的书写、物质制备实验方案设计的评价以及有机物的推断,需要学生对反应信息理解运用,注意推断中根据J的结构与转化关系中反应条件判断,注意掌握官能团的性质与转化,难度中等.


科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 容器里气体的密度为40g•L-1 | |
| B. | SO3的分解率为20% | |
| C. | 化学反应速率v(Ag2SO4)=v(SO3) | |
| D. | 在这10min内的平均反应速率为v(O2)=0.005mol•L-1•min-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 电离平衡常数可以表示弱电解质的相对强弱 | |
| B. | 电离平衡常数受溶液浓度的影响 | |
| C. | H2CO3的电离常数表达式:K=$\frac{c({H}^{+})•c(C{O}_{3}^{2-})}{c({H}_{2}C{O}_{3})}$ | |
| D. | 电离常数大的酸溶液中c(H+)一定比电离常数小的酸中大 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 化学式 | CH3COOH | H2C2O4 | H2S |
| 电离平衡常数 | 1.8×10-5 | Ka1=5.4×10-2 Ka2=5.4×10-5 | Ka1=1.3×10-7 Ka2=7.1×10-15 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
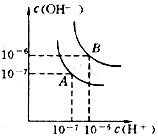 水的电离平衡线如图所示.若以A点表示25℃时水在电离平衡时的离子浓度,当温度上升到100℃时,水的电离平衡状态到B点
水的电离平衡线如图所示.若以A点表示25℃时水在电离平衡时的离子浓度,当温度上升到100℃时,水的电离平衡状态到B点查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com