
观察是研究物质性质的一种基本方法.一同学将一小块金属钠露置于空气中,观察到下列现象:银白色 变灰暗
变灰暗 变白色
变白色 出现液滴
出现液滴 白色固体,下列说法正确的是( )
白色固体,下列说法正确的是( )
|
| A. | ①发生了氧化还原反应 |
|
| B. | ②变白色是因为生成了碳酸钠 |
|
| C. | ③是碳酸钠吸收空气中的水蒸气形成了溶液 |
|
| D. | ④只发生物理变化 |
| 钠的化学性质;钠的重要化合物. | |
| 专题: | 几种重要的金属及其化合物. |
| 分析: | 根据Na、Na2O、NaOH以及Na2CO3等物质的性质以及化学反应类型来回答. |
| 解答: | 解:Na的性质活泼,易与空气中氧气反应生成Na2O,Na2O易与水反应生成NaOH,NaOH吸收空气中的水和CO2生成 Na2CO3•xH2O,Na2CO3•xH2O风化脱水生成Na2CO3, A、金属钠氧化为氧化钠的反应属于氧化还原反应,故A正确; B、Na2O易与水反应生成NaOH,②变白色是因为生成了氢氧化钠,故B错误; C、③是NaOH吸收空气中的水和CO2生成Na2CO3•xH2O,故C错误; D、Na2CO3•xH2O风化脱水生成Na2CO3属于化学变化,故D错误. 故选A. |
| 点评: | 本题考查钠及钠的重要化合物的性质,题目难度不大,注意相关基础知识的积累. |


科目:高中化学 来源: 题型:
下列实验操作中正确的是( )
A.制取溴苯:将铁屑、溴水、苯混合加热
B.实验室制取硝基苯:先加入浓硫酸,再加苯,最后滴入浓硝酸
C.鉴别甲苯和苯:向甲苯和苯中分别滴入酸性KMnO4溶液,振荡,观察是否褪色
D.通过向溴水中加入乙醇来萃取溴水中的溴
查看答案和解析>>
科目:高中化学 来源: 题型:
甲、乙、丙、丁四种物质中,甲、乙、丙均含有相同的某种元素,它们之间具有如下转化关系: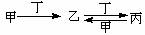 。下列有关物质的推断不正确的是( )
。下列有关物质的推断不正确的是( )
A.若甲为焦炭,则丁可能是O2 B.若甲为SO2,则丁可能是氨水
C.若甲为Fe,则丁可能是盐酸 D.若甲为NaOH溶液,则丁可能是CO2
查看答案和解析>>
科目:高中化学 来源: 题型:
用NA表示阿伏伽德罗常数的值.下列叙述正确的组合是( )
①14g乙烯和丙烯的混合物中氢原子数为2NA个
②0.1mol•L﹣1的FeCl3溶液滴入沸水形成的胶体粒子的数目为0.1NA个
③标准状况下,2.24L Cl2通入足量的NaOH溶液中转移的电子数为0.1NA个
④25℃时,pH=13的1.0L Ba(OH)2溶液中含有的OH﹣ 数目为0.2NA个
⑤常温下,100mL 1mol•L﹣1Na2CO3溶液中阴离子总数大于0.1NA个
⑥1mol Na2O2与足量水蒸气反应转移电子数为NA个
⑦常温下,2.7g铝片投入足量的浓硫酸中,铝失去的电子数为0.3NA个.
A.①④⑤⑦ B. ②⑤⑥⑦ C. ①③⑤⑥ D. ①③⑤⑦
查看答案和解析>>
科目:高中化学 来源: 题型:
98%的浓硫酸(密度为1.84g•cm﹣3)配制0.5mol•L﹣1的稀硫酸180mL,现给出下列仪器(配制过程中可能用到):①50mL量筒;②10mL量筒;③50mL烧杯;④托盘天平;⑤250mL容量瓶;⑥胶头滴管;⑦玻璃棒.配置过程一定需要使用的仪器是( )
|
| A. | ②③⑤⑥⑦ | B. | ③④⑤⑥⑦ | C. | ①②③⑤⑥⑦ | D. | ①③⑤⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列中学化学中常见物质的转化关系如图,反应条件及部分反应物和产物未全部注明,已知A、D为金属单质,其他为化合物.
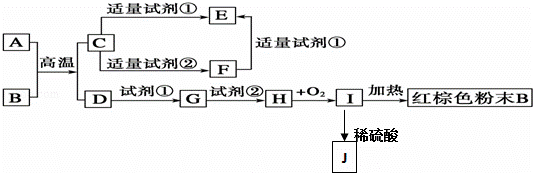
(1)写出B的化学式 ;
(2)写出反应A+B→C+D的一种应用 ;
(3)写出过量的D与稀硝酸反应的离子方程式: ;
(4)H→I的化学方程式: ;
(5)某同学认为物质J 中可能同时含有同一金属元素的不同价态,若要确定其中低价阳离子的存在最好应选用 ;
A、KSCN溶液和氯水 B、铁粉和KSCN 溶液C、浓氨水 D、KMnO4溶液.
查看答案和解析>>
科目:高中化学 来源: 题型:
已知:H2(g)+F2(g)===2HF(g) 的能量变化如图所示,下列有关叙述中正确的是
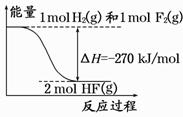
A.氟化氢气体分解生成氢气和氟气的反应是放热反应
B.1 mol H2与1 mol F2反应生成2 mol液态HF放出的热量小于270 kJ
C.在相同条件下,1 mol H2与1 mol F2的能量总和大于2 mol HF气体的能量
D.断裂1 mol H—H键和1 mol F—F 键放出的能量大于形成2 mol H—F键放出的能量
查看答案和解析>>
科目:高中化学 来源: 题型:
氨基甲酸铵(NH2COONH4)是一种白色固体,易分解、易水解,可用做肥料、灭火剂、洗涤剂等。某化学兴趣小组模拟工业原理制备氨基甲酸铵,
反应的化学方程式如下:2NH3(g)+CO2(g)  NH2COONH4(s) ΔH<0
NH2COONH4(s) ΔH<0
(1)如用右图装置制取氨气,你所选择的试剂是 。

(2)制备氨基甲酸铵的装置如下图所示,把氨气和二氧化碳通入四氯化碳中,不断搅拌混合,生成的氨基甲酸铵小晶体悬浮在四氯化碳中。当悬浮物较多时,停止制备。
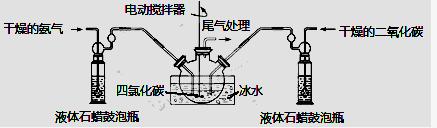
注:四氯化碳与液体石蜡均为惰性介质。
①发生器用冰水冷却的原因是: 、 。液体石蜡鼓泡瓶的作用是: 。
②从反应后的混合物中分离出产品,为了得到干燥产品,应采取的方法是_______ (填写选项序号)。
a.常压加热烘干 b.高压加热烘干 c.真空40 ℃以下烘干
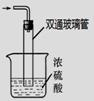
③尾气处理装置如右图所示。双通玻璃管的作用: ;
浓硫酸的作用: 、 。
(3)取因部分变质而混有碳酸氢铵的氨基甲酸铵样品11.73 g,用足量石灰水 充分处理后,使碳元素完全转化为碳酸钙,过滤、洗涤、干燥,测得质量为15.00 g。则样品中氨基甲酸铵的物质的量分数为 。
[Mr(NH2COONH4)=78g/mol、Mr(NH4HCO3) =79 g/mol、Mr(CaCO3)=100 g/mol]【来.源:全,】
查看答案和解析>>
科目:高中化学 来源: 题型:
氨基甲酸铵(NH2COONH4)是一种白色固体,易分解、易水解,可用做肥料、灭火剂、洗涤剂等。某化学兴趣小组模拟工业原理制备氨基甲酸铵,
反应的化学方程式如下:
2NH3(g)+CO2(g)  NH2COONH4(s) ΔH<0
NH2COONH4(s) ΔH<0
(1)如用右图装置制取氨气,你所选择的试剂是 。

(2)制备氨基甲酸铵的装置如下图所示,把氨气和二氧化碳通入四氯化碳中,不断搅拌混合,生成的氨基甲酸铵小晶体悬浮在四氯化碳中。当悬浮物较多时,停止制备。

注:四氯化碳与液体石蜡均为惰性介质。
①发生器用冰水冷却的原因是: 、 。液体石蜡鼓泡瓶的作用是: 。
②从反应后的混合物中分离出产品,为了得到干燥产品,应采取的方法是_______ (填写选项序号)。
a.常压加热烘干 b.高压加热烘干 c.真空40 ℃以下烘干
③尾气处理装置如右图所示。双通玻璃管的作用: ;
浓硫酸的作用: 、 。

(3)取因部分变质而混有碳酸氢铵的氨基甲酸铵样品11.73 g,用足量石灰水 充分处理后,使碳元素完全转化为碳酸钙,过滤、洗涤、干燥,测得质量为15.00 g。则样品中氨基甲酸铵的物质的量分数为 。
[Mr(NH2COONH4)=78g/mol、Mr(NH4HCO3) =79 g/mol、Mr(CaCO3)=100 g/mol]【来.源:全,
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com