
【题目】硫代硫酸钠(![]() )是常用的还原剂。在一定体积的某维生素C(化学式
)是常用的还原剂。在一定体积的某维生素C(化学式![]() )溶液中加入
)溶液中加入![]() 溶液
溶液![]() ,使维生素C完全氧化,充分反应后,用
,使维生素C完全氧化,充分反应后,用![]() 溶液滴定剩余的I2,消耗
溶液滴定剩余的I2,消耗![]() 溶液
溶液![]() 。
。
已知发生的反应为: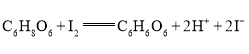
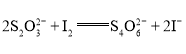 ,该溶液中维生素C的物质的量是__________mol。写出简要的计算过程__________。
,该溶液中维生素C的物质的量是__________mol。写出简要的计算过程__________。
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】人们对苯及芳香烃的认识有一个不断深化的过程,回答下列问题:
(1)已知分子式为C6H6的有机物有多种,其中的两种为:(Ⅰ)![]() (Ⅱ)
(Ⅱ)![]() 。
。
①这两种结构的区别表现在以下两方面:
定性方面(即化学性质方面):(Ⅱ)能发生的反应___(填字母),而(Ⅰ)不能。
a.被高锰酸钾酸性溶液氧化 b.与溴水发生加成反应
c.与溴发生取代反应 d.与氢气发生加成反应
定量方面(即消耗反应物的量的方面):
1molC6H6与H2加成时:(Ⅰ)需要H2__mol,而(Ⅱ)需要H2__mol。
②今发现C6H6还可能有一种如图![]() 所示的立体结构,该结构的二氯代物有__种。
所示的立体结构,该结构的二氯代物有__种。
(2)如图是制取溴苯的装置,试回答:
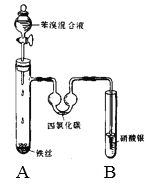
①装置A中发生反应的化学方程式是:____。
②装置B中盛有硝酸银溶液,实验中看到的现象是:___,证明有___生成,说明反应属于___反应(填写反应类型)。
③反应完毕后,将具支试管中的混合液倒入装有水的烧杯中,然后加___溶液后,可除去了其中的溴。写出除溴的化学方程式:___。
④苯易取代,难加成。请写出苯发生硝化反应的方程式:____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】含苯酚的工业废水处理的流程如下图。

(1)上述流程里,设备Ⅰ中进行的是操作______(填写操作名称)。实验室里这一步操作可以用__________进行(填写仪器名称)。
(2)由设备Ⅱ进入设备Ⅲ的物质A是__________,由设备Ⅲ进入设备Ⅳ的物质B是_________。
(3)在设备Ⅲ中发生反应的化学方程式为__________。
(4)在设备Ⅳ中,物质B的水溶液和CaO反应后,产物是NaOH、H2 O和__________。通过__________操作(填操作名称),可以使产物相互分离。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下,在体积固定的密闭容器中通入2.0 mol SO2、1.2molO2,发生反应2SO2(g) + O2(g)![]() 2SO3(g) ΔH= -198 kJ·mol - 1,下列判断不正确的是( )
2SO3(g) ΔH= -198 kJ·mol - 1,下列判断不正确的是( )
A.2SO2(g) + O2(g) ![]() 2SO3(s) ΔH< -198kJ·mol-1
2SO3(s) ΔH< -198kJ·mol-1
B.增加反应物的量不能改变上述反应的ΔH
C.充分反应后,放出的热量小于198 kJ
D.若从反应开始到建立平衡放出热量158.4 kJ,则SO2的平衡转化率为60%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】溶液中的反应X+3Y![]() 2Z分别在①、②、③三种不同实验条件下进行,它们的起始浓度为c(X)=c(Y)=0.100molL-1、c(Z)=0molL-1,反应物X的浓度随时间变化如图所示。②、③与①比较只有一个实验条件不同,下列说法不正确的是
2Z分别在①、②、③三种不同实验条件下进行,它们的起始浓度为c(X)=c(Y)=0.100molL-1、c(Z)=0molL-1,反应物X的浓度随时间变化如图所示。②、③与①比较只有一个实验条件不同,下列说法不正确的是
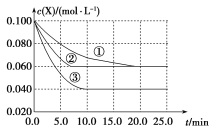
A.反应0~5.0min实验③的反应速率最快B.条件②的反应最先达到平衡
C.②与①比较,②可能压强更大D.该反应的正反应是吸热反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I2在KI溶液中存在下列平衡:I2(aq)+I-(aq)![]() I3-(aq)。某I2、KI混合溶液中,I3-的物质的量浓度[c(I3-)]与温度(T)的关系如图所示(曲线上任何一点都表示平衡状态)。下列说法正确的是( )
I3-(aq)。某I2、KI混合溶液中,I3-的物质的量浓度[c(I3-)]与温度(T)的关系如图所示(曲线上任何一点都表示平衡状态)。下列说法正确的是( )

A. 反应I2(aq)+I-(aq)=I3-(aq)的ΔH>0
B. 若温度为T1、T2,反应的平衡常数分别为K1、K2,则K1>K2
C. 若反应进行到状态D时,一定有v正<v逆
D. 状态A与状态B相比,状态A的c(I2)大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.在下列事实中,影响化学反应速率的因素分别为:
(1)夏天将食物存放在电冰箱里___;
(2)钠可以与冷水剧烈反应,铝与水反应必须加热____;
(3)工业制氨需要高压____。
Ⅱ.向体积为2L的恒容密闭容器中充入1molN2和3molH2,发生反应N2(g)+3H2(g)![]() 2NH3(g),达到平衡时,N2的转化率为20%,回答下列问题:
2NH3(g),达到平衡时,N2的转化率为20%,回答下列问题:
(1)平衡时,c(N2):c(H2)=___,平衡转化率α(N2):α(H2)=___;
(2)设平衡时压强为P平,反应开始时压强为P始,则P平:P始=___;
(3)若起始投料改为只加入2molNH3,则相同条件达到平衡时NH3的转化率为α(NH3)=__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】制取氨气并完成喷泉实验(图中夹持装置均已略去)。
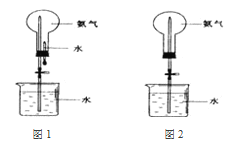
(1)写出实验室用氯化铵和氢氧化钙制取氨气的化学方程式________。
(2)收集氨气应用_____法,要得到干燥的氨气可选用_______做干燥剂。
(3)用图1装置进行喷泉实验,上部烧瓶已装满干燥氨气,引发水上喷的操作是___________。该实验的原理是_________________。
(4)如果只提供如图2的装置,请说明引发喷泉的方法________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国是煤炭消费大国,高硫煤(主要含FeS2)在我国煤炭消费中占有相当大的比例,其燃烧时产生的SO2对环境和人体健康造成了一定的负面影响,所以运用电化学法进行煤的燃前脱硫是一项具有前景的技术。已知:2FeS2+7O2+8NaOH=2Fe(OH)2+4Na2SO4+2H2O,图甲是模拟电化学法脱硫的示意图(电极均为惰性电极),对此方法说法不正确的是
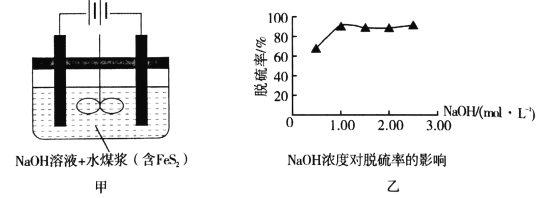
A.将煤制成水煤浆加入电解槽有利于反应的充分进行
B.阳极的电极反应式为4OH--4e-=O2↑+2H2O
C.煤中的铁元素最终以Fe(OH)2的形式存在
D.根据图乙中的信息,NaOH溶液的适宜浓度为1mol/L
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com