
| A. | 醛基的结构简式-COH | B. | 丙烯分子的结构简式为:CH3CHCH2 | ||
| C. | 四氯化碳分子的电子式为: | D. | 2-乙基-1,3-丁二烯的键线式: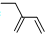 |
分析 A.醛基中存在碳氧双键,醛基的结构简式应该为:-CHO;
B.丙烯分子中含有碳碳双键,结构简式中不能漏掉碳碳双键;
C.四氯化碳的电子式中没有标出氯离子的最外层的3对孤对电子;
D.将碳、氢元素符号省略,只表示分子中键的连接情况,每个拐点或终点均表示有1个碳原子,称为键线式,据此判断该有机物结构简式,然后进行命名.
解答 解:A.醛基正确的结构简式为-CHO,故A错误;
B.丙烯分子中含有碳碳双键,丙烯正确的结构简式为CH3CH=CH2,故B错误;
C.四氯化碳为共价化合物,分子中存在4个碳氯键,碳原子和氯原子都达到8电子稳定结构,四氯化碳正确的电子式为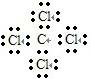 ,故C错误;
,故C错误;
D.2-乙基-1,3-丁二烯分子中,在1、3号碳各含有一个碳碳双键,在2号C含有一个乙基,其键线式为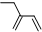 ,故D正确;
,故D正确;
故选D.
点评 本题考查了常见的化学用语的表示方法判断,题目难度中等,涉及电子式、键线式、结构简式等知识,注意掌握常见的化学用语的书写原则,试题有利于培养学生的规范答题能力.


科目:高中化学 来源: 题型:选择题

| A. | 铜是阳极,铜片上有气泡产生 | |
| B. | 铜离子在铜片表面被还原 | |
| C. | 电流从锌片经导线流向铜片 | |
| D. | 反应中,盐桥中的K+会移向ZnSO4溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
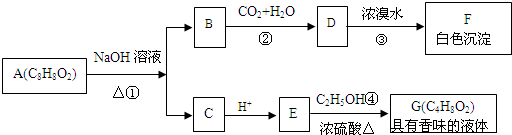
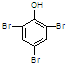 ;
;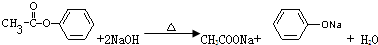 ;
;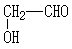 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 将某无色气体通入品红溶液中,品红溶液褪色,则此气体一定是SO2 | |
| B. | 取少许某溶液并滴加数滴硫氰化钾溶液,无明显现象,再滴加数滴H2O2溶液,溶液变血红色,则原溶液中一定含Fe2+ | |
| C. | 在硫酸钡沉淀中加入浓碳酸钠溶液充分搅拌后,取沉淀(洗净)放入盐酸中有气泡产生,说明Ksp(BaCO3)<Ksp(BaSO4) | |
| D. | 在淀粉溶液中加入稀硫酸并加热片刻再加入适量银氨溶液,水浴加热后没有银镜生成,说明淀粉没有水解 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
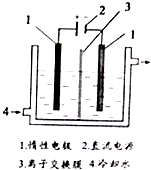 碘被称为“智力元素”,科学合理地补充碘可防止碘缺乏病.碘酸钾(KIO3)是国家规定的食盐加碘剂,它的晶体为白色,可溶于水.碘酸钾在酸性介质中与过氧化氢或碘化物作用均生成单质碘.以碘为原料,通过电解制备碘酸钾的实验装置如图所示.请回答下列问题:
碘被称为“智力元素”,科学合理地补充碘可防止碘缺乏病.碘酸钾(KIO3)是国家规定的食盐加碘剂,它的晶体为白色,可溶于水.碘酸钾在酸性介质中与过氧化氢或碘化物作用均生成单质碘.以碘为原料,通过电解制备碘酸钾的实验装置如图所示.请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
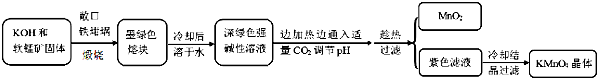
| 物质 | KMnO4 | K2CO3 | KHCO3 | K2SO4 | CH3COOK |
| 20℃溶解度 | 6.4 | 111 | 33.7 | 11.1 | 217 |

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
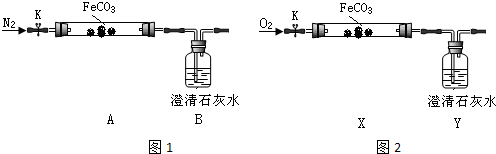
| 实验编号 | 实验步骤 | 实验现象 |
| i | 向甲溶液滴加KSCN溶液 | 溶液变红色 |
| ii | 向乙溶液滴加酸性高锰酸钾溶液 | 溶液不褪色 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 左下方区域的金属元素 | B. | 金属和非金属分界线附近的元素 | ||
| C. | 过渡元素 | D. | 稀有气体元素 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
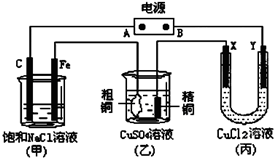 如图所示的装置,X、Y都是惰性电极.将电源接通后,向(甲)中滴入酚酞溶液,在Fe极附近显红色.试回答下列问题:
如图所示的装置,X、Y都是惰性电极.将电源接通后,向(甲)中滴入酚酞溶液,在Fe极附近显红色.试回答下列问题:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com