
 ,
, ;
;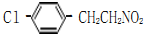 、
、 、
、
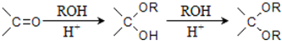
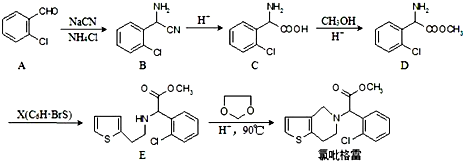
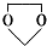 的合成路线流程图(无机试剂任选).
的合成路线流程图(无机试剂任选). 分析 (1)母体为苯甲醛,氯原子处于苯环2号位置;由C的结构可知,含有的官能团有羧基、氨基、氯原子;
(2)对比C、D的结构可知,C中羧基与醇发生酯化反应;由D、E的结构可知,D→E发生取代反应,对比D、E的结构确定X的结构;
(3)旋转碳碳单键可以使-CN处于平衡平面内;
(4)两分子C可在一定条件下反应生成一种产物,该产物分子中含有3个六元环,应是氨基与羧基之间发生脱水反应,两分子C脱去2分子水生成 ;
;
(5)物质C的某种同分异构体G满足以下条件:a.为芳香族化合物且分子结构中含一个硝基(-NO2),
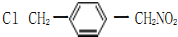
b.核磁共振氢谱有四组峰,且面积之比为 1:1:1:1,取代基为-Cl、-CH2CH2NO2,或者-NO2、-CH2CH2Cl,或者-CH2Cl、-CH2NO2,均处于对位位置;
(6)乙烯与溴发生加成反应生成1,2-二溴乙烷,再发生水解反应生成乙二醇,甲醇催化氧化生成HCHO,最后乙二醇与甲醛反应生成 .
.
解答 解:(1)母体为苯甲醛,氯原子处于苯环2号位置,A的名称为2-氯苯甲醛,由C的结构可知,含有的官能团有羧基、氨基、氯原子,
故答案为:2-氯苯甲醛;羧基、氨基、氯原子;
(2)对比C、D的结构可知,C中羧基与醇发生酯化反应,也属于取代反应,由D、E的结构可知,D→E发生取代反应,对比D、E的结构确定X的结构简式为: ,
,
故答案为:取代(或酯化); ;
;
(3)旋转碳碳单键可以使-CN处于平衡平面内,故B分子中最多有14个原子共面,
故答案为:14;
(4)两分子C可在一定条件下反应生成一种产物,该产物分子中含有3个六元环,应是氨基与羧基之间发生脱水反应,两分子C脱去2分子水生成 ,反应方程式为:
,反应方程式为: ,
,
故答案为: ;
;
(5)物质C的某种同分异构体G满足以下条件:a.为芳香族化合物且分子结构中含一个硝基(-NO2),
b.核磁共振氢谱有四组峰,且面积之比为 1:1:1:1,取代基为-Cl、-CH2CH2NO2,或者-NO2、-CH2CH2Cl,或者-CH2Cl、-CH2NO2,均处于对位位置,可能的结构简式为: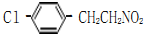 、
、 、
、 ,
,
故答案为: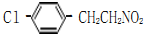 、
、 、
、 ;
;
(6)乙烯与溴发生加成反应生成1,2-二溴乙烷,再发生水解反应生成乙二醇,甲醇催化氧化生成HCHO,最后乙二醇与甲醛反应生成 ,合成路线流程图为:
,合成路线流程图为: ,
,
故答案为: .
.
点评 本题考查有机物的推断与合成、有机反应类型、限制条件同分异构体书写等,是对有机化学基础的综合考查,充分利用有机物的结构进行分析解答,较好的考查学生分析推理能力,难度中等.


 赢在课堂名师课时计划系列答案
赢在课堂名师课时计划系列答案科目:高中化学 来源: 题型:多选题
| A. | 容器中CO2、H2、CH3OH、H2O的物质的量之比为1:3:1:1 | |
| B. | v正(CO2)=v逆(H2O) | |
| C. | 容器内混合气体密度保持不变 | |
| D. | 3molH-H键断裂同时断裂3molH-O键 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
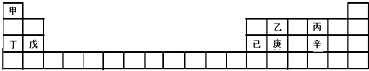
| A. | 甲、丁、戊的单质都是金属 | |
| B. | 乙、丙、辛都是非金属元素 | |
| C. | 乙、庚、辛都能形成氧化物 | |
| D. | 已的氧化物既可溶于KOH溶液又可溶于H2SO4溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
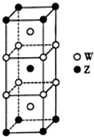 短周期元素T、X、Y、Z的原子序数依次增大,其中元素T、X基态原子均有2个未成对电子,元素Y基态原子s能级的电子总数与p能级的电子总数相等,元素Z的价电子数等于能层数.元素W位于第四周期,其基态原子所含未成对电子数在该周期中最多.
短周期元素T、X、Y、Z的原子序数依次增大,其中元素T、X基态原子均有2个未成对电子,元素Y基态原子s能级的电子总数与p能级的电子总数相等,元素Z的价电子数等于能层数.元素W位于第四周期,其基态原子所含未成对电子数在该周期中最多.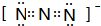 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
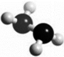 肼(N2H4)是火箭燃料,常温下为液体,其分子的球棍模型如图所示.肼能与双氧水发生反应:N2H4+2H2O2═N2+4H2O.下列说法正确的是( )
肼(N2H4)是火箭燃料,常温下为液体,其分子的球棍模型如图所示.肼能与双氧水发生反应:N2H4+2H2O2═N2+4H2O.下列说法正确的是( )| A. | 标准状况下,11.2L N2H4中含共用电子对数为2.5NA | |
| B. | 1mol N2H4和1mol H2O2含有的电子总数不相等 | |
| C. | 若生成3.6g H2O,则上述反应转移电子的数目为0.2 NA | |
| D. | N2H4和H2O2均只含有极性共价键 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
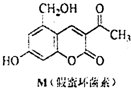 天然化合物M(假蜜环菌素)的结构简式如图所式.对M的结构与性质叙述错误的是( )
天然化合物M(假蜜环菌素)的结构简式如图所式.对M的结构与性质叙述错误的是( )| A. | M的分子式为C12H10O5 | |
| B. | M能发生取代反应、加成反应、氧化反应、还原反应 | |
| C. | M中碳原子之间全部以C-C键或C=C键相互结合 | |
| D. | M的同分异构体最多含有2个与乙酸相同的官能团 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 往碳酸镁中滴加稀盐酸:CO32-+2H+═CO2↑+H2O | |
| B. | 浓烧碱溶液中加入铝片:Al+2OH-═AlO2-+H2↑ | |
| C. | 氯化钙与碳酸氢钾溶液混合:Ca2++CO32-═CaCO3↓ | |
| D. | 用惰性电极电解氯化镁溶液:Mg2++2Cl-+2H2O$\frac{\underline{\;电解\;}}{\;}$Cl2↑+H2↑+Mg(OH)2↓ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | X元素可以组成多种单质 | |
| B. | Y和Z可能在同一周期 | |
| C. | X与W形成的化合物和Z与W形成的化合物的化学键类型不同 | |
| D. | 元素X、Y、W的最高价氧化物对应水化物的酸性强弱:X<Y<W |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com