
����Ԫ���������о�Ԫ�ؼ��仯��������ʾ�����Ҫ�����壮
I�����ֶ���������Ԫ�ص�����������Ӧ��ˮ���Ũ�Ⱦ�Ϊ0.01mol��L-1����Һ��PH��ԭ�������Ĺ�ϵ��ͼ��ʾ��
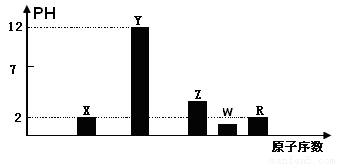
��1��Ԫ��R�����ڱ��е�λ����
��2��Ԫ��Y��W�γɵ�Y2W2�ͻ������к��л�ѧ��������Ϊ
��3����д��X������������Ӧ��ˮ����������̬�⻯������ӷ�Ӧ����ʽ
������Ԫ��C��O��S���γɶ��ֻ������CO2��CS2��COS��
��1��������˵��̼��������Ԫ�طǽ��������ǿ������ ������ţ�
A��S��H2�������Ϸ�Ӧ��C��H2���ϸ�����
B�����ԣ�H2SO3��H2CO3
C���ȶ��ԣ�CH4��H2S
��2���ʻ���COS������Ϊһ��Ѭ�������ܷ�ֹijЩ���桢�߳��Σ��������ӽṹ��CO2����
���ʻ���COS���ĵ���ʽΪ��
���ʻ���COS��������������Һ���������õĹ������£�
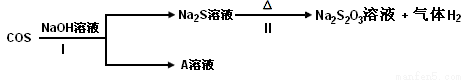
��֪A��һ�����Σ���ӦI�Ļ�ѧ��Ӧ����ʽΪ

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2016-2017ѧ���������������ʡ��У�߶���ѧ�����л�ѧ�Ծ��������棩 ���ͣ�ѡ����
��֪��ӦC��ʯī�� C�����ʯ�� ��H>0�������ж���ȷ���ǣ� ��
C�����ʯ�� ��H>0�������ж���ȷ���ǣ� ��
A��ʯī�Ƚ��ʯ�ȶ� B��12 g���ʯ��������12 gʯī�ĵ�
C�����ʯ��ʯī�ȶ� D�����ʯ��ʯī�����ת��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016-2017ѧ�긣��ʡ�߶������л�ѧ���������棩 ���ͣ��ƶ���
�ֶ�����Ԫ��A��B��C��D��ԭ��������������C��Dλ��ͬ������ԭ���������8����̬Aԭ�Ӻ�����3���ܼ������ɵ�����ÿ���ܼ��ϵ�������ȣ�Cԭ��s�ܼ�����������p�ܼ���������ȣ���̬Eԭ�ӵ�M������2��δ�ɶԵ������չ����
��1����̬Eԭ�ӵļ۲���ӹ����ʾʽΪ ��
��2��Ԫ��A��B��C�ĵ�һ�������ɴ�С����Ϊ (��Ԫ�ط��ű�ʾ)
��3��AC32-������ԭ���ӻ�����Ϊ ��DC32-�Ŀռ乹��Ϊ ��
��4����֪(DAB)2�����к��Ǽ��Լ���������ÿ��ԭ������㶼�ﵽ8�������ȶ��ṹ��1mol(DAB)2���Ӻ��Ҽ�����ĿΪ �� д��һ����DAB-���ӻ�Ϊ�ȵ�����ķ��� (�ѧʽ)
��5�������E(AC)4�ڳ����³�Һ̬�����������Ȼ�̼�������л��ܼ�����̬E(AC)4�ľ��������� ��
��6���˹��ϳɵ�EC�������ȱ�ݣ�����������+3��+2�����֡�ij���˺ϳɵľ�����Ʒ���ΪE0.96C����þ�����+3�ۡ�+2���������ӵĸ���֮��Ϊ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016-2017ѧ�긣��ʡ�߶������л�ѧ���������棩 ���ͣ�ѡ����
���ۼ������Ӽ��ͷ��»�������������֮��IJ�ͬ���������������ʣ���Na2O2����SiO2����ʯī���ܽ��ʯ����CaH2���ް��ף����к�����������������
A���٢ۢ� B���ڢܢ� C���٢ڢۢ� D���٢ۢݢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016-2017ѧ�긣��ʡ�߶������л�ѧ���������棩 ���ͣ�ѡ����
�����Ӳ���ʹ���������ɫ��ԭ����
A�������в����ڦм� B�������д���6���Ӵ�м�,�ṹ�ȶ�
C��������ƽ��ṹ D��������ֻ���ڦҼ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016-2017ѧ�꽭��ʡ������ʮ��У�߶���ѧ�����л�ѧ�Ծ��������棩 ���ͣ�ѡ����
һ����������2L���ܱ������У�����2mol SO2��1molO2������Ӧ:2SO2��g�� + O2��g��  2SO3��g����H=��196kJ•moL-1��������������ʵ�������0.8molʱ��Ӧ�ﵽƽ�⣬�����й���������ȷ���ǣ�
2SO3��g����H=��196kJ•moL-1��������������ʵ�������0.8molʱ��Ӧ�ﵽƽ�⣬�����й���������ȷ���ǣ�  ��
��
A�������¶Ȳ��䣬��ƽ�����������ٳ���1molSO2��0.5molO2ʱ��V(��)��V(�棩
B����ͬ�¶��£���ʼʱ�������г���2mol SO3����ƽ��ʱSO3��ת����Ϊ20%
C��ƽ����������S02�����ʵ���Ϊ1.2mol
D�����������������䣬����ʼʱ�������г���2molSO3����ƽ��ʱ����39.2kJ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016-2017ѧ�꽭��ʡ������ʮ��У�߶���ѧ�����л�ѧ�Ծ��������棩 ���ͣ�ѡ����
��֪����101kPaʱ��2C(s)+O2��g�� 2CO��g����H=��221kJ/mol
2CO��g����H=��221kJ/mol
��ϡ��Һ�У�H+��aq��+OH��(aq) H2O��
H2O�� l����H=��57.3kJ/mol�����н�����ȷ���ǣ� ��
l����H=��57.3kJ/mol�����н�����ȷ���ǣ� ��
A��̼��ȼ����Ϊ110.5 kJ/mol
B���ٵķ�Ӧ��Ϊ221 kJ/mol
C��ϡ������ϡNaOH��Һ��Ӧ����1 molˮ���ų�������Ϊ57.3 kJ
D��ϡ������ϡNaOH��Һ��Ӧ���к���Ϊ57.3 kJ/mol
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016-2017ѧ�꼪��ʡ��Դ�и�һ��ѧ�����л�ѧ���������棩 ���ͣ�ѡ����
�������з�Ӧ�ж�����������������ǿ������˳����ȷ����
��Cl2+2KI�TI2+2KCl
��2FeCl3+2HI�TI2+2FeCl2+2HCl
��2FeCl2+Cl2�T2FeCl3
��I2+SO2+2H2O�T2HI+H2SO4��
A��Cl2��I2��FeCl3��H2SO4 B��FeCl3��Cl2��I2��H2SO4
C��Cl2��FeCl3��H2SO4��I2 D��Cl2��FeCl3��I2��H2SO4
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016-2017ѧ�����ʡ¦���е���У��һ�����л�ѧ���������棩 ���ͣ�ѡ����
��ͳ�ƣ�ȫ��ÿ90���Ӿ���1�ָ�������ʴ��ÿ����1.3�ڶָ�������ʴ������ɾ�ľ�����ʧ�������ڳ�ʪ�Ŀ����з�����ʴ�������� ���䷴Ӧ�Ļ�ѧ����ʽΪ��
���䷴Ӧ�Ļ�ѧ����ʽΪ��
��2Fe+O2+2H2O = 2Fe(OH)2��
��4Fe(OH)2+O2+2H2O = 4Fe(OH)3��
��2Fe(OH)3 = Fe2O3+3H2O
����������Ӧ�У����ڷ�������ԭ��Ӧ���ǣ� ��
A���٢� B���٢� C���٢ڢ� D����
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com