
| A. | 溴水中:Na+、K+、SiO32-、CO32- | |
| B. | pH=13的溶液:Ba2+、Na+、I-、ClO- | |
| C. | 苯酚钠溶液中:HSO3-、K+、Na+、AlO2- | |
| D. | 加入淀粉碘化钾溶液显蓝色:Na+、NH4+、SO42-、CH3COO- |
分析 A.溴水中不能存在弱酸根离子;
B.pH=13的溶液,显碱性,离子之间发生氧化还原反应;
C.苯酚钠溶液显碱性;
D.加入淀粉碘化钾溶液显蓝色,具有氧化性物质,与该组离子均不反应.
解答 解:A.溴水中不能存在SiO32-、CO32-,故A不选;
B.pH=13的溶液,显碱性,I-、ClO-发生氧化还原反应,故B不选;
C.苯酚钠溶液显碱性,不能大量存在HSO3-,且HSO3-、AlO2-结合生成沉淀,故C不选;
D.加入淀粉碘化钾溶液显蓝色,具有氧化性物质,与该组离子均不反应,可大量共存,故D选;
故选D.
点评 本题考查离子的共存,为高频考点,把握习题中的信息及常见离子之间的反应为解答的关键,侧重分析与应用能力的考查,注意复分解反应、氧化还原反应的判断,题目难度不大.


科目:高中化学 来源: 题型:推断题
 +Br2→
+Br2→ ;
; ;
; .
. .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | H2SO4溶于水能形成H+和SO42-,说明H2SO4是离子化合物 | |
| B. | HCl气体溶于水,HCl分子里共价键被破坏 | |
| C. | 单质分子中不存在化学键,化合物分子中才存在化学键 | |
| D. | 含金属元素的离子一定是阳离子 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
| 实验步骤 | 实验现象 |
| ①将镁条用砂纸打磨后,放入试管中,加入少量水后,加热至水沸腾;再向溶液中滴加酚酞溶液 | A.浮在水面上,熔成小球,四处游动,发出“嘶嘶”声,随之消失,溶液变成红色. |
| ②向新制得的Na2S溶液中滴加新制的氯水 | B.有气体产生,溶液变成浅红色 |
| ③将一小块金属钠放入滴有酚酞溶液的冷水中 | C.剧烈反应,迅速产生大量无色气体. |
| ④将镁条投入稀盐酸中 | D.反应不十分剧烈;产生无色气体. |
| ⑤将铝条投入稀盐酸中 | E.生成白色胶状沉淀,继而沉淀消失 |
| ⑥向A1Cl3溶液中滴加NaOH溶液至过量 | F.生成淡黄色沉锭. |
| 实验内容 | ① | ② | ③ | ④ | ⑤ | ⑥ |
| 实验现象(填A~F) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.5mol•L-1•min-1 | B. | 1 mol•L-1•min-1 | ||
| C. | 4 mol•L-1•min-1 | D. | 2 mol•L-1•min-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
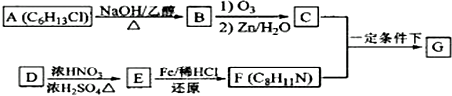


 +HO-NO2$→_{△}^{浓H_{2}SO_{4}}$
+HO-NO2$→_{△}^{浓H_{2}SO_{4}}$ +H2O.
+H2O. .
. (写出其中一种的结构简式).
(写出其中一种的结构简式).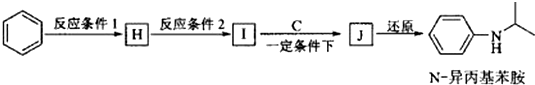
 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com