
| A. | N | B. | O | C. | Na | D. | S |
分析 W、X、Y、Z为原子序数依次增大的四种短周期元素,由每三种元素组成的化合物:WXZ、WXY能抑制水的电离,则为酸或碱,W为H,X为O,XYZ的化合物中有一种和WYZ的化合物能促进水的电离,则为促进水解的盐,盐可能为NaHS,NaClO,可知Y为Na,Z为S,且四种元素组成的两种化合物可发生反应生成能使品红溶液褪色的气体,气体为二氧化硫,以此来解答.
解答 解:W、X、Y、Z为原子序数依次增大的四种短周期元素,由每三种元素组成的化合物:WXZ、WXY能抑制水的电离,则为酸或碱,W为H,X为O,XYZ的化合物中有一种和WYZ的化合物能促进水的电离,则为促进水解的盐,盐可能为NaHS,NaClO,可知Y为Na,Z为S,且四种元素组成的两种化合物可发生反应生成能使品红溶液褪色的气体,即硫酸氢钠与亚硫酸氢钠反应生成气体为二氧化硫,具有漂白性,则Y为Na符合题意,
故选C.
点评 本题考查位置、结构与性质的关系,为高频考点,把握促进或抑制水电离的物质及二氧化硫的漂白性为解答的关键,侧重分析与推断能力的考查,题目难度中等.


科目:高中化学 来源: 题型:选择题
| A. | 能够发生有效碰撞的分子叫做活化分子,活化分子所多出的那部分能量称作活化能 | |
| B. | 对于某一反应aA+bB=cC+dD,△H单位中的mol-1是指每摩尔(aA+bB=cC+dD)反应 | |
| C. | 研究有机物的组成、结构、性质、制备方法与应用的科学叫有机化学 | |
| D. | 甲烷分子具有正四面体结构的原因是碳原子的2S轨道与2P轨道发生SP杂化 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 钠跟水反应:2Na+2H2O═2Na++2OH-+H2↑ | |
| B. | 铁粉跟稀硫酸反应:2Fe+6H+═2Fe3++3H2↑ | |
| C. | 氢氧化钡溶液跟稀硫酸反应:Ba2++SO42-═BaSO4↓ | |
| D. | 碳酸钙跟盐酸反应:CO32-+2H+═H2O+CO2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
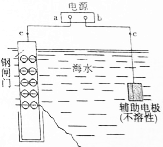 金属是日常生活和工农业生产中广泛使用的材料.恰当的金属防腐方法是延长金属材料使用寿命的前提.
金属是日常生活和工农业生产中广泛使用的材料.恰当的金属防腐方法是延长金属材料使用寿命的前提.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 质量相同时,分子数相同 | B. | 同温同压下,密度相同 | ||
| C. | 体积相同时,分子数相同 | D. | 质量相等时,原子数相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
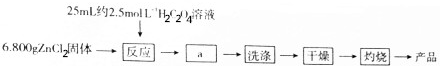
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
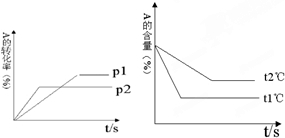 回答下列问题
回答下列问题查看答案和解析>>
科目:高中化学 来源: 题型:选择题
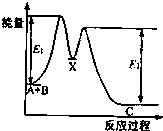 反应A+B→C分两步进行:①A+B→X;②X→C.反应过程中能量变化如图所示.下列有关叙述正确的是( )
反应A+B→C分两步进行:①A+B→X;②X→C.反应过程中能量变化如图所示.下列有关叙述正确的是( )| A. | E2表示反应X→C的反应热 | |
| B. | A+B→C此反应放热 | |
| C. | X是反应A+B→C的催化剂 | |
| D. | 加入催化剂可改变反应A+B→C的反应热 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com