
分析 (1)同周期元素从左到右第一电离能逐渐增大,但同周期第ⅡA和第ⅤA主族比相邻的元素第一电离能都要大,同主族从上往下逐渐减小;
(2)电负性大小与非金属性的强弱一致,根据电负性的变化规律作答;
(3)能层序数相同时,能级越高,能量越高;能级符号相同时,能层序数越大,能量越高,以此规律判断.
解答 解:(1)同一周期元素中,元素的第一电离能随着原子序数的增大而增大,Mg和Al位于同一周期,且Al位于第ⅢA族、Mg位于第ⅡA族,Mg的价电子排布式为3s2全满稳定,所以第一电离能Mg>Al.
故答案为:>;
(2)同周期元素自左到右电负性逐渐增大,所以电负性O<F,F是电负性最大的元素.
故答案为:<;
(3)能层序数相同时,能级越高,能量越高,故ns<np,
故答案为:<.
点评 本题考查第一电离能、电负性、能量变化的递变规律,熟知这些规律和特例是解题的基础,题目难度不大.


科目:高中化学 来源: 题型:实验题
 如图为实验室制备乙烯的装置图,请回答:
如图为实验室制备乙烯的装置图,请回答:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
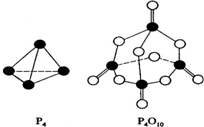 (1)CH3-CH3(g)→CH2=CH2(g)+H2(g);有关化学键的键能如下.
(1)CH3-CH3(g)→CH2=CH2(g)+H2(g);有关化学键的键能如下.| 化学键 | C-H | C=C | C-C | H-H |
| 键能(kJ/mol) | 414.4 | 615.3 | 347.4 | 435.3 |
| 化学键 | P-P | P-O | P=O | O-O | O=O |
| 键能(kJ/mol) | a | b | c | d | e |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
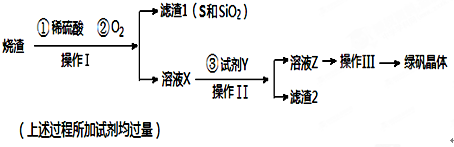
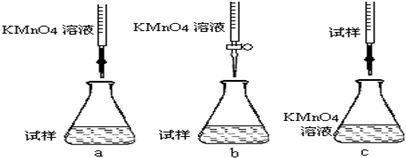
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 第一电离能由大到小的顺序为O>N>C | |
| B. | NO3-中N采用sp2杂化,故NO3-的空间构型为三角锥形 | |
| C. | 由于C22-和O22+为等电子体,所以可以判断O22+的电子式为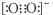 | |
| D. | 液态HF通常也可以写成(HF)n的形式,是因为液态HF分子间存在氢键 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 反应混合物的浓度改变 | B. | 反应混合物的压强改变 | ||
| C. | 正、逆反应速率改变 | D. | 反应物的转化率改变 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com