
下表是元素周期表的一部分,表中所列的字母分别代表一种化学元素。
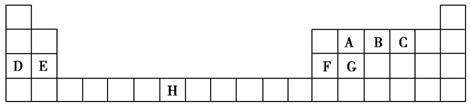
试回答下列问题:
(1)B、D、F、G的第一电离能由小到大的顺序为______(用元素符号表示)。
(2)请写出元素H的基态原子电子排布式_____________________。
(3)A的最简单氢化物分子里中心原子采取________形式杂化,A的最高价氧化物分子的空间构型是________。
(4)D的氯化物的熔点比G的氯化物的熔点________(填“高”或“低”),理由是__________________________。
(5)元素C与元素G形成的晶体所属的晶体类型为________晶体,在该晶体中原子间形成的共价键属于________(从下列选项中选出正确类型)。
A.σ键 B.π键 C.既有σ键,又有π键
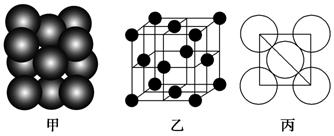
(6)F单质晶体中原子的堆积方式如图甲所示,其晶胞特征如图乙所示,原子之间相互位置关系的平面图如图丙所示。晶胞中F原子的配位数为________,一个晶胞中F原子的数目为________。
(共11分) (1)Na<Al<Si<N(1分)
(2)1s22s22p63s23p63d54s2(或[Ar]3d54s2)(1分)
(3)sp3(1分) 直线形(1分)
(4)高 (1分)NaCl为离子晶体,而SiCl4为分子晶体(2分)
(5)原子(1分) A (1分) (6)12(1分) 4(1分)
【解析】(1)非金属性越强,第一电离能越大。所以大小顺序是Na<Al<Si<N。
(2)H是锰元素,根据构造原理可知,基态原子电子排布式为1s22s22p63s23p63d54s2(或[Ar]3d54s2)。
(3)碳的最简单氢化物是甲烷,由于碳原子中没有孤对电子,所以是正四面体形结构,采用sp3杂化。碳的最高价氧化物是CO2,属于直线型结构。
(4)钠的氯化物是氯化钠,形成的晶体是离子晶体,熔点高。硅的氯化物是四氯化碳,形成的晶体是分子晶体,熔点低。
(5)硅和氧形成的氧化物是二氧化硅,形成的晶体是原子晶体。硅原子和氧原子全部以单键相连,所以是σ键,答案选A。
(6)F是Al,根据晶胞的结构可知,配位数是3×8÷2=12。含有的原子数是8×1/8+6×1/2=4。


 小学课时特训系列答案
小学课时特训系列答案科目:高中化学 来源: 题型:
主族 周期 |
ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | ① | ② | ③ | |||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ |


查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
| A | B | C | D | E | |||||||||||||
| F | G | H | |||||||||||||||
| I | J | K | |||||||||||||||
| L | |||||||||||||||||
| M | N | ||||||||||||||||
| O | |||||||||||||||||
查看答案和解析>>
科目:高中化学 来源: 题型:
| a | b | ||||||||||||||||
| c | d | ||||||||||||||||
| e | f | g | h | ||||||||||||||
| i | |||||||||||||||||
| j | |||||||||||||||||


 NH4++OH-,试判断NH3溶于水后,形成的NH3?H2O的合理结构是
NH4++OH-,试判断NH3溶于水后,形成的NH3?H2O的合理结构是 (4)1906年的诺贝尔化学奖授予为制备F2单质作出重要贡献的化学家莫瓦桑,请预测首先被用来与F2反应制备稀有气体化合物的元素是
(4)1906年的诺贝尔化学奖授予为制备F2单质作出重要贡献的化学家莫瓦桑,请预测首先被用来与F2反应制备稀有气体化合物的元素是查看答案和解析>>
科目:高中化学 来源: 题型:
| 周期 主族 | IA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅥⅠA | 0 |
| 2 | C | N | O | F | ||||
| 3 | Na | Mg | Si | S | Cl | Ar | ||
| 4 | Ca |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com