
| A. | 氯乙烯、溴乙烯 | B. | 乙烯、乙炔 | C. | 乙烷、乙烯 | D. | 苯、2-丁烯 |
 金牌课堂练系列答案
金牌课堂练系列答案 三新快车金牌周周练系列答案
三新快车金牌周周练系列答案科目:高中化学 来源: 题型:选择题
| A. | 人类目前所直接利用的能量大部分是由化学反应产生的 | |
| B. | 煤、石油、天然气是当今世界最重要的三种化石燃料 | |
| C. | 化学变化中的能量变化主要是由化学键变化引起的 | |
| D. | 化学反应中能量变化的大小与反应物的质量多少无关 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 在一体积为10L的容器中,通入一定量的CO和H2O,850℃时发生反应:CO(g)+H2O(g)?CO2(g)+H2(g).CO和H2O浓度变化如图所示:
在一体积为10L的容器中,通入一定量的CO和H2O,850℃时发生反应:CO(g)+H2O(g)?CO2(g)+H2(g).CO和H2O浓度变化如图所示:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | F、Cl、Br、I最高价氧化物对应水化物的酸性依次减弱 | |
| B. | 多电子原子中,在离核较近的区域内运动的电子能量较高 | |
| C. | 元素原子的最外层电子数等于元素的最高化合价 | |
| D. | Na、Mg、Al失电子能力和最高价氧化物对应水化物的碱性均依次减弱 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ②③④⑤ | B. | ②⑤⑥ | C. | ② | D. | ②⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
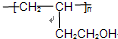 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
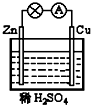
| A. | 正极反应为 Cu-2e-Cu2+ | B. | 溶液中H+向锌片移动 | ||
| C. | 电子由锌片通过导线流向铜 | D. | 该装置能将电能转化为化学能 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | H2XO3 | B. | H2YO4 | C. | HZO4 | D. | H3RO4 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com