
【题目】已知室温下氨水中存在如下平衡:NH3H2O![]() NH4++OH-,在5份0.01mol·L-1
NH4++OH-,在5份0.01mol·L-1
的氨水中分别加入下列各物质:A、浓氨水B、纯水C、少量NaOH固体D、少量浓硫酸E、NH4Cl固体,按照要求填空:
(1)电离平衡会向逆向移动是___。
(2)c(NH4+)、c(OH-)都增大的是___,升温时氨水的Kb将___(填“增大”、“减小”或“不变”)。
(3)c(NH4+)增大,c(OH-)减小的是___。
(4)在25℃下,将amol·L-1的氨水与0.01mol·L-1的盐酸等体积混合,反应平衡时溶液中c(NH4+)=c(Cl-)。则溶液显___性(填“酸”“碱”或“中”);用含a的代数式表示NH3·H2O的电离常数Kb=___。
【答案】C、E A 增大 D、E 中 ![]()
【解析】
氨水中存在:NH3H2ONH4++OH-,加水稀释促进一水合氨电离,加入含有铵根离子或氢氧根离子的物质抑制一水合氨电离,加入和铵根离子或氢氧根离子反应的物质促进一水合氨电离,据此分析。
![]() 加入少量氢氧化钠,
加入少量氢氧化钠,![]() 增大抑制一水合氨电离,加入少量氯化铵,
增大抑制一水合氨电离,加入少量氯化铵,![]() 增大,抑制一水合氨电离,所以抑制一水合氨电离的是CE,故答案为:CE;
增大,抑制一水合氨电离,所以抑制一水合氨电离的是CE,故答案为:CE;
![]() 向溶液中加入浓氨水,一水合氨电离平衡正向移动,溶液中
向溶液中加入浓氨水,一水合氨电离平衡正向移动,溶液中![]() 、
、![]() 都增大;物质的电离都是吸热的,升高温度,会促进氨水的电离,氨水的
都增大;物质的电离都是吸热的,升高温度,会促进氨水的电离,氨水的![]() 将增大,故答案为:A;增大;
将增大,故答案为:A;增大;
![]() 向溶液中加入少量浓硫酸,硫酸电离出的氢离子会中和掉氢氧根离子,促进一水合氨的电离,铵根离子浓度增大;向溶液中加入氯化铵,铵根离子浓度增大抑制一水合氨电离,则氢氧根离子浓度减小,故答案为:DE;
向溶液中加入少量浓硫酸,硫酸电离出的氢离子会中和掉氢氧根离子,促进一水合氨的电离,铵根离子浓度增大;向溶液中加入氯化铵,铵根离子浓度增大抑制一水合氨电离,则氢氧根离子浓度减小,故答案为:DE;
![]() 在 25
在 25 ![]() 下 , 平衡时溶液中
下 , 平衡时溶液中 ![]() , 根据物料守恒得
, 根据物料守恒得 ![]()
![]() , 根据电荷守恒得
, 根据电荷守恒得 ![]() , 溶液呈中性 ,
, 溶液呈中性 ,![]()
![]() 的电离常数
的电离常数 。
。


 七星图书口算速算天天练系列答案
七星图书口算速算天天练系列答案 初中学业考试导与练系列答案
初中学业考试导与练系列答案科目:高中化学 来源: 题型:
【题目】过碳酸钠( Na2CO4)是一种很好的供氧剂,其与稀盐酸反应的化学方程式为:2Na2CO4+4HCl=4NaCl+2CO2 +O2+2H2O.市售过碳酸钠一般都含有碳酸钠,为测定某过碳酸钠样品(只含Na2CO4和Na2CO3)的纯度,某化学兴趣小组采用以下两种方案实施:
方案一:![]()
(1)操作①和③的名称分别为
(2)上述操作中,使用到玻璃棒的有 __(填操作序号)。
(3)请简述操作③的操作过程
方案二:按下图安装好实验装置,Q为一塑料气袋,随意取适量样品于其中,打开分液漏斗活塞,将稀盐酸滴入气袋中至充分反应。

(4)为测定反应生成气体的总体积,滴稀盐酸前必须关闭 ,打开 (填“K1”、“K2”或“K3”)。导管a的作用是 。
(5)当上述反应停止后,使K1、K3处于关闭状态,K2处于打开状态,再缓缓打开Kl。 B中装的固体试剂是 ,为何要缓缓打开K1? 。
(6)实验结束时,量筒I中有xmL水,量筒Ⅱ中收集到了ymL气体,则样品中过碳酸钠的质量分数是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】![]() 中国诗词大会
中国诗词大会![]() 不仅弘扬了中华传统文化,诗句中还蕴含着许多化学知识.下列分析正确的是
不仅弘扬了中华传统文化,诗句中还蕴含着许多化学知识.下列分析正确的是![]()
A.“忽闻海上有仙山,山在虚无缥缈间”的海市蜃楼是一种自然现象,与胶体知识无关
B.“千淘万漉虽辛苦,吹尽狂沙始到金”说明金的化学性质稳定,在自然界中常以单质状态存在
C.“纷纷灿烂如星陨,霍霍喧逐似火攻.”灿烂美丽的烟花是某些金属的焰色反应,属于化学变化
D.“日照香炉生紫烟,遥看瀑布挂前川”中的“烟”是弥漫在空气中的![]() 固体颗粒
固体颗粒
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组离子一定能在指定环境中大量共存的是
A.在c(H+)=10-10 mol/L的溶液中 Al3+、NH![]() 、Cl-、NO
、Cl-、NO![]()
B.pH值为1的溶液 Fe2+、Na+ 、SO42-、NO![]()
C.水电离出来的c(H+)=10-12mol/L的溶液 K+、HCO3-、Cl-、ClO-
D.pH值为13的溶液 K+、CO![]() 、Na+、[Al(OH)]4-
、Na+、[Al(OH)]4-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:①298K时K(HF)=3.5×10-4,Ksp(CaF2)=1.8×10-7
②HF(aq)![]() H+(aq)+F-(aq)△H<0
H+(aq)+F-(aq)△H<0
根据以上已知信息判断下列说法正确的是( )
A. 298K时,加蒸馏水稀释HF溶液, ![]() 保持不变
保持不变
B. 308K时,HF的电离常数Ka>3.5×10-4
C. 298K时,向饱和CaF2溶液中加入少量CaCl2,Ksp(CaF2)会减小
D. 2HF(aq)+Ca2+(aq)![]() CaF2(s)+2H+(aq)K≈0.68
CaF2(s)+2H+(aq)K≈0.68
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关化学反应速率和化学平衡影响的图象,其中图象和实验结论表达错误的是




A. a是其他条件一定时,反应速率随温度变化的图象,正反应ΔH > 0
B. b是在有无催化剂存在下建立的平衡过程图象,Ⅰ是使用催化剂时的曲线
C. c是一定条件下,向含有一定量A的容器中逐渐加入B时的图象,压强p1 > p2
D. d是在平衡体系的溶液中溶入少量KCl固体后化学反应速率随时间变化的图象
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)甘氨酸的结构简式为![]() ,其中含氧官能团的名称是____________,该物质是____________性化合物。
,其中含氧官能团的名称是____________,该物质是____________性化合物。
(2)以乙炔、HCl等有关试剂在一定条件下合成聚氯乙烯的流程如下:
![]()
①指出反应Ⅱ的反应类型是____________。
②写出反应I的化学方程式________________________________
(3)1 mol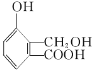 最多能与________________mol NaOH发生反应。
最多能与________________mol NaOH发生反应。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学兴趣小组欲利用MnO2和浓盐酸及如图所示装置制备Cl2。下列分析中不正确的是
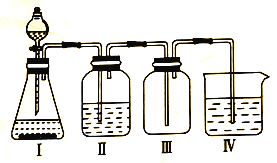
A.I中缺少加热装置
B.Ⅱ为净化Cl2的装置,其盛放的是NaOH溶液
C.Ⅲ为收集Cl2的装置
D.Ⅳ中处理多余的Cl2时,Cl2既作氧化剂,又作还原剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学小组为了研究外界条件对化学反应速率的影响,进行了酸性高锰酸钾与草酸(H2C2O4)的反应,记录如表所示的实验数据:
实验 编号 | 实验 温度 | 试管中所加试剂及其用量/mL | 溶液褪至无 色所需时间 /min | |||
0.6mol/L H2C2O4 溶液 | H2O | 3mol/L H2SO4 | 0.05mol/L KMnO4 | |||
① | 25 | 3.0 | V1 | 2.0 | 3.0 | 1.5 |
② | 25 | 2.0 | 3.0 | 2.0 | 3.0 | 2.7 |
③ | 50 | 2.0 | V2 | 2.0 | 3.0 | 1.0 |
(1)请写出该反应的离子方程式 ______,当该反应以表中数据反应完全时转移电子数为______NA。
(2)V1=_______mL。
(3)根据表中的实验①、②数据,可以得到的结论是 _______。
(4)探究温度对化学反应速率的影响,应选择 _______(填实验编号)
(5)该小组根据经验绘制了n(Mn 2+)随时间变化的趋势如图1所示,但有同学查阅已有实验资料发现,该实验过程中n(Mn 2+)随时间变化的实际趋势如图2所示。
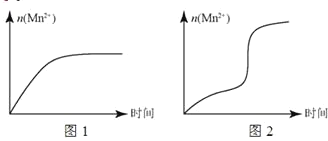
该小组同学根据图 2 所示信息提出了新的假设,并设计实验方案④继续进行实验探究。
实验温度 /℃ | 试管中所加试剂及其用量 | 再加入某种固体 | 溶液褪至无色所需时间/min | ||||
0.6mol/L H2C2O4 | H2O | 3mol/L H2SO4 | 0.05mol/L KMnO4 | ||||
④ | 25 | 2.0 | 3.0 | 2.0 | 3.0 | MnSO4 | t |
①小组同学提出的假设是________。
②若该小组同学提出的假设成立,应观察到________现象。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com